题目内容
9.老师为同学们提供了如下实验装置: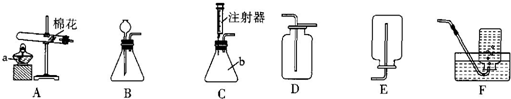
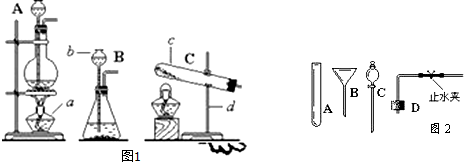
(1)写出仪器a、b的名称:a是酒精灯,b是锥形瓶.
(2)实验室用高锰酸钾制取氧气,应选用的发生装置是A (填字母序号,下同).该反应的符号表达式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑若要收集较纯的氧气,可选用的装置是F.
(3)实验室也可选用过氧化氢溶液和二氧化锰在装置B中制取氧气,该反应的符号表达式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.若选用C做发生装置,你认为选用装置C的优点是够控制反应速率,节约药品.(与装置B做比较)
(4)已知氨气(NH3)是一种密度比空气小且极易溶于水的有毒气体,其水溶液称为氨水.实验室常用加热氯化铵和氢氧化钙的固体混合物来制取氨气,则制取氨气应选用的发生装置是A,收集装置E.
(5)用氯酸钾和二氧化锰制取氧气的符号表达式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;铁丝在氧气中燃烧的符号表达式3Fe+2O2 $\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
分析 (1)认识常见实验仪器;
(2)根据反应物的状态和反应条件来选择发生装置;根据排水法和向上排空气法各自的优点来分析;
(3)根据过氧化氢在二氧化锰的催化作用下分解为水和氧气来书写;
(4)根据实验室制取氨气的反应物和反应条件选择发生装置;并依据氨气的性质选择合适的收集装置;
(5)根据氯酸钾制取氧气的反应原理书写方程式;
解答 解:(1)仪器a是酒精灯;仪器b是锥形瓶;故答案为:酒精灯;锥形瓶;
(2)实验室用高锰酸钾制取氧气需要加热,应该用A装置作为发生装置;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,该反应的符号表达式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;排水法收集的氧气比较纯净;向上排空气法收集到的氧气比较干燥;
(3)过氧化氢在二氧化锰作催化剂的条件下,分解生成水和氧气,该反应的符号表达式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.选用装置C的优点是能够控制反应速率,节约药品;
(4)实验室常用氯化铵固体与碱石灰固体共热来制取氨气,所以选择A发生装置;由于氨气密度比空气小,所以可用向下排空气法收集;
(5)氯酸钾以二氧化锰为催化剂加热生成氯化钾和氧气,方程式是:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,铁丝在氧气中燃烧生成了四氧化三铁,反应的符号表达式是:3Fe+2O2 $\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
答案:
(1)a酒精灯;b锥形瓶;
(2)A;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;F;
(3)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;够控制反应速率,节约药品;
(4)A;E;
(5)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;3Fe+2O2 $\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
点评 本考点主要考查气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案| A. | 只有分子 | B. | 质子、中子、电子 | C. | 只有原子 | D. | 分子、原子和离子 |
| A. | 2Fe+6HCl═2FeCl3+3H2↑ | B. | Fe2O3+4HCl═2FeCl2+3H2O | ||
| C. | Na2CO3+2HNO3═2NaNO3+H2O+CO2↑ | D. | Zn+2HNO3═Zn(NO3)2+H2↑ |
| A. |  滴加液体 | B. |  倾倒液体 | C. | 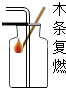 验满氧气 | D. | 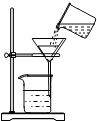 过滤 |
 X、Y、Z、R、W、A、B是初中化学常见的八种纯净物,它们均由碳、氢、氧、硫、钠、铜中的一种或多种元素组成.
X、Y、Z、R、W、A、B是初中化学常见的八种纯净物,它们均由碳、氢、氧、硫、钠、铜中的一种或多种元素组成. 探究燃烧条件的实验装置如图所示.
探究燃烧条件的实验装置如图所示.