题目内容
13.选择正确的物质用序号填空:A氢气、B生石灰、C一氧化碳、D消石灰、E氧气、F浓硫酸、G二氧化碳、H纯碱.(1)能供人体呼吸的气体是E;
(2)相对分子质量最小的气体是A;
(3)用于改良酸性土壤的物质是D;
(4)能还原氧化铜的氧化物是C;
(5)用作食品干燥剂的物质是B;
(6)其固体能用于人工降雨的是G.
分析 物质的性质决定物质的用途,根据已有的物质的性质进行分析解答即可.
解答 解:(1)氧气能帮助呼吸,能供人体呼吸的气体是氧气;
(2)相对分子质量最小的气体是氢气;
(3)消石灰即氢氧化钙,可以与酸反应,用于改良酸性土壤;
(4)一氧化碳具有还原性,能还原氧化铜;
(5)氧化钙能与水反应,常用食品作干燥剂;
(6)二氧化碳固体是干冰,升华吸热,能用于人工降雨.
答案:(1)E;(2)A;(3)D;(4)C;(5)B;(6)G.
点评 掌握常见的物质的性质是正确解答本题的关键.生活处处有化学,学会用所学的化学知识去解决生活中的实际问题.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
3.下列各组物质在给定pH的溶液中能大量共存并形成无色溶液是( )
| A. | pH为3:FeCl3、CuSO4、NaCl | B. | pH为12:BaCl2、Na2C03、NaOH | ||
| C. | pH为4:NaOH、NaHCO3、K2SO4 | D. | pH为1:NH4Cl、Na2SO4、HNO3 |
2.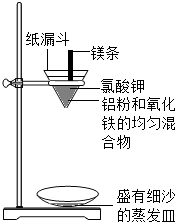 铝粉和氧化铁粉末反应(铝热反应).实验装置如图:
铝粉和氧化铁粉末反应(铝热反应).实验装置如图:
图中纸漏斗由两张滤纸折叠成漏斗状套在一起,使四周都有四层,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中.
实验后老师作了如下提示:实验中镁条和氯酸钾的作用是提供反应所需的高温条件,铝粉和氧化铁粉末在高温条件下的反应叫铝热反应,属于置换反应,该反应常用于焊接钢轨.请写出该反应的化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.该反应中单质铝与一氧化碳有相似的还原(填“氧化”或“还原”)性.在这一实验过程中没有涉及的基本反应类型是复分解反应.
实验后同学们对金属与金属氧化物间的反应产生兴趣,激发了探究热情.
【提出问题】任何金属与金属氧化物在高温条件下都能反应吗?
同学们在请教老师后设计了如下实验方案并进行了探究.
【实验方案】
【实验总结】金属与金属氧化物在高温条件下有些能反应,有些不能反应.
 铝粉和氧化铁粉末反应(铝热反应).实验装置如图:
铝粉和氧化铁粉末反应(铝热反应).实验装置如图:图中纸漏斗由两张滤纸折叠成漏斗状套在一起,使四周都有四层,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中.
实验后老师作了如下提示:实验中镁条和氯酸钾的作用是提供反应所需的高温条件,铝粉和氧化铁粉末在高温条件下的反应叫铝热反应,属于置换反应,该反应常用于焊接钢轨.请写出该反应的化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.该反应中单质铝与一氧化碳有相似的还原(填“氧化”或“还原”)性.在这一实验过程中没有涉及的基本反应类型是复分解反应.
实验后同学们对金属与金属氧化物间的反应产生兴趣,激发了探究热情.
【提出问题】任何金属与金属氧化物在高温条件下都能反应吗?
同学们在请教老师后设计了如下实验方案并进行了探究.
【实验方案】
| 实验组别 | 实验操作 | 实验现象 | 结论 |
| 实验1 | 取Zn、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 黑色粉末变成红色固体部分溶解,有气泡产生,水溶液呈无色. | Zn和CuO能发生置换反应. |
| 实验2 | 取Mg、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 发生爆炸,黑色粉末变成红色. 固体部分溶解,有气泡产生,水溶液呈无色. | Mg和CuO能反应 |
| 实验3 | 取Cu、Fe2O3粉末的均匀混合物于密闭容器中,高温加热. | 粉末无变化 | Cu、Fe2O3不能反应. |
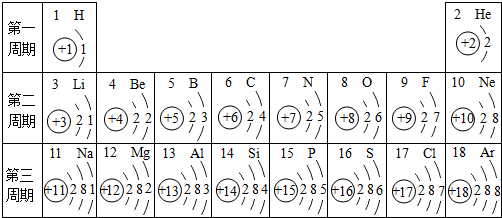
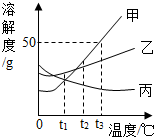 如图所示,依据甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
如图所示,依据甲、乙、丙三种固体物质的溶解度曲线,回答下列问题: