题目内容
在C、Mg、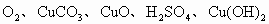 7种物质中选取适当的反应物,按下列要求写出相关的化学反应方程式(每种物质只能使用一次)
7种物质中选取适当的反应物,按下列要求写出相关的化学反应方程式(每种物质只能使用一次)
(1)化合反应(生成固体)________
(2)分解反应(没有单质生成)________
(3)置换反应(生成固体单质)________
(4)中和反应________
答案:
解析:
解析:
|
(1)2Mg+ (2) (3)C+2CuO (4) |

练习册系列答案
相关题目
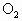
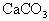
 ↑
↑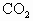
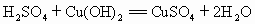
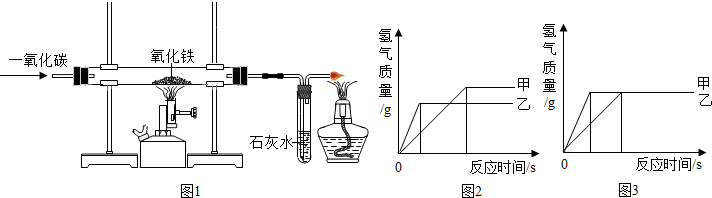
 7种物质中,选择适当的反应物,按下列要求写出相关的化学方程式(每种物质只能使用一次).
7种物质中,选择适当的反应物,按下列要求写出相关的化学方程式(每种物质只能使用一次).