题目内容
工业上常用NaOH溶液处理铝土矿(主要成分Al2O3),反应的化学方程式:Al2O3+2NaOH═2NaAlO2+H2O.欲对含Al2O3 204t的铝土矿进行处理(杂质不参与反应),理论上需要消耗NaOH的质量为多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据Al2O3与NaOH反应的化学方程式,由氧化铝的质量可以计算氢氧化钠的质量;
解答:解:设需要消耗NaOH的质量为x,
Al2O3+2NaOH=2NaAlO2+H2O
102 80
204t x
=
x=160t
答:需要消耗NaOH的质量是160t.
Al2O3+2NaOH=2NaAlO2+H2O
102 80
204t x
| 102 |
| 204t |
| 80 |
| x |
x=160t
答:需要消耗NaOH的质量是160t.
点评:本题考查的是有关化学方程式的计算问题,考查内容简单注重基础,需熟练掌握计算步骤和格式即可解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
N(NO2)3是科学家2011年发现的一种新型火箭推进剂的原料.有关说法正确的是( )
| A、N(NO2)3由三种元素组成 |
| B、N(NO2)3属于酸 |
| C、N(NO2)3的相对分子质量152 |
| D、N(NO2)3中氮元素的质量分数为18.4% |
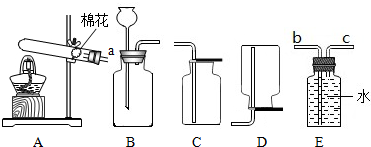
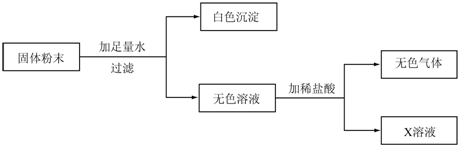
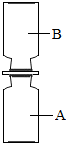 体味化学魅力,尽享实验神奇.化学老师在元旦化学晚会上表演了神奇的化学实验,请大家一起参与.
体味化学魅力,尽享实验神奇.化学老师在元旦化学晚会上表演了神奇的化学实验,请大家一起参与.