题目内容
20.将下列固体加入稀硫酸中,溶液的酸性不会明显减弱的是( )| A. | Zn | B. | BaCl2 | C. | NaOH | D. | CaO |
分析 锌和稀硫酸反应生成硫酸锌和氢气,氯化钡和稀硫酸反应生成硫酸钡沉淀和稀盐酸,氢氧化钠和稀硫酸反应生成硫酸钠和水,氧化钙和稀硫酸反应生成硫酸钙和水.
解答 解:A、锌和稀硫酸反应生成硫酸锌和氢气,随着反应的进行,溶液的酸性会明显减弱;
B、氯化钡和稀硫酸反应生成硫酸钡沉淀和稀盐酸,由于反应生成盐酸,因此随着反应的进行,溶液的酸性不会明显减弱;
C、氢氧化钠和稀硫酸反应生成硫酸钠和水,随着反应的进行,溶液的酸性会明显减弱;
D、氧化钙和稀硫酸反应生成硫酸钙和水,随着反应的进行,溶液的酸性会明显减弱.
故选:B.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列除去杂质的方法中,正确的是( )
| A. | 除去铜粉中混有的铁:加足量稀硝酸,过滤 | |
| B. | 除去N2中少量的CO:通过足量灼热的CuO粉末 | |
| C. | 除去KCl溶液中的少量CaCl2:加适量Na2CO3溶液,过滤 | |
| D. | 除去CO2中的少量的HCl:通过足量的饱和碳酸氢钠溶液 |
15.世界卫生组织将ClO2列为高效灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有广泛用途.下列有关分析正确的是( )
| A. | 二氧化氯是由二个氧原子和一个氯原子构成的 | |
| B. | 二氧化氯中氯元素的化合价为-1价 | |
| C. | 二氧化氯是氧化物 | |
| D. | 氯元素与氧元素的质量之比为1:2 |
5.鉴别如表物质的方法不正确的是( )
| 选项 | 鉴别的物质 | 鉴别的方法 |
| A | 冰和干冰 | 室温(20℃)放置一会,观察是否有痕渍 |
| B | 水和双氧水 | 加二氧化锰,观察是否有气泡 |
| C | 硬水和软水 | 加入肥皂水,观察产生泡沫的多少 |
| D | 二氧化锰和四氧化三铁 | 观察颜色 |
| A. | A | B. | B | C. | C | D. | D |
12.如图粒子在化学反应中容易失去电子的是( )
| A. |  | B. |  | C. |  | D. | 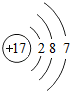 |
4.小明在家中探究食用白醋的性质,选用了家庭生活中的下列常见物品:200ml的软透明塑料瓶、食品干燥剂、白醋、鸡蛋壳、紫罗兰花、锈铁钉、蒸馏水、纯碱、玻璃小杯.
【问题】白醋是否具有酸类的性质?
【查阅资料】
(1)白醋为无色透明液体,主要成分是醋酸,化学式可表示为HAc,Ac-代表醋酸根;
(2)食品干燥剂的主要成分是氧化钙;
(3)紫罗兰花遇酸变为红色;
(4)醋酸盐中除银盐和汞盐外都易溶解于水.
【探究与验证】(请你帮助填写表中空白)
【反思与评价】
(1)小明将干燥剂袋口打开一段时间后,袋中的白色颗粒粘在了一起,请写出变化的化学方程式:①CaO+H2O═Ca(OH)2
②Ca(OH)2+CO2═CaCO3↓+H2O
(2)上面“实验结论”中,错误的是(填实验序号)四.
(3)上述实验三的现象还不足以得出表中所述的相应结论,为此还需要补充相应的实验,写出补充实验发生反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
【问题】白醋是否具有酸类的性质?
【查阅资料】
(1)白醋为无色透明液体,主要成分是醋酸,化学式可表示为HAc,Ac-代表醋酸根;
(2)食品干燥剂的主要成分是氧化钙;
(3)紫罗兰花遇酸变为红色;
(4)醋酸盐中除银盐和汞盐外都易溶解于水.
【探究与验证】(请你帮助填写表中空白)
| 序号 | 实验操作 | 实验现象 | 实验结论 |
| 一 | 将白醋滴在紫罗兰花上 | 紫罗兰花变红 | 白醋的pH<7 |
| 二 | 将锈铁钉放在小玻璃杯中,加入白醋 | 刚开始时铁锈溶解,溶液由无色变成黄色,一段时间后,有气泡冒出. | 1.白醋能与铁锈反应 2.白醋能与铁反应 |
| 三 | 向软塑料瓶中加入10ml白醋,将瓶捏扁,加入约5g鸡蛋壳,拧紧瓶盖 | 瓶中有气泡冒出,扁塑料瓶逐渐膨胀 | 白醋能与碳酸钙反应放出CO2 |
| 四 | 向白醋中加入纯碱 | 白醋中有气泡冒出 | 白醋能与碱反应 |
(1)小明将干燥剂袋口打开一段时间后,袋中的白色颗粒粘在了一起,请写出变化的化学方程式:①CaO+H2O═Ca(OH)2
②Ca(OH)2+CO2═CaCO3↓+H2O
(2)上面“实验结论”中,错误的是(填实验序号)四.
(3)上述实验三的现象还不足以得出表中所述的相应结论,为此还需要补充相应的实验,写出补充实验发生反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
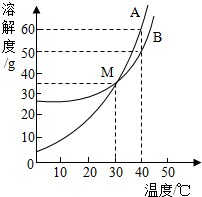 A、B两种物质的溶解度曲线如图.
A、B两种物质的溶解度曲线如图.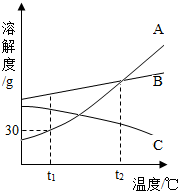 如图是A、B、C三种物质的溶解度曲线,跟据如图回答:
如图是A、B、C三种物质的溶解度曲线,跟据如图回答: