题目内容
5.一包白色粉末可能由CaCO3、Na2SO4、CuSO4、Na2CO3中的一种或几种组成,将少量该粉末加入足量水中,下列根据现象得出的结论不正确的是( )| A. | 溶液呈无色,则一定没有硫酸铜 | |
| B. | 溶液澄清透明,则一定没有碳酸钙 | |
| C. | 向该溶液中加入氯化钡溶液,生成白色沉淀,则一定有硫酸钠和碳酸钠 | |
| D. | 向上述白色沉淀中加入足量稀硝酸,无现象,则白色固体中一定没有碳酸钠 |
分析 A、根据硫酸铜在溶液中显蓝色进行分析;
B、根据碳酸钙难溶于水进行分析;
C、根据碳酸钠、硫酸钠和氯化钡都会生成白色沉淀进行分析;
D、根据碳酸钠和硝酸反应会生成二氧化碳气体进行分析.
解答 解:A、硫酸铜在溶液中显蓝色,溶液呈无色,则一定没有硫酸铜,故A正确;
B、碳酸钙难溶于水,溶液澄清透明,则一定没有碳酸钙,故B正确;
C、碳酸钠、硫酸钠和氯化钡都会生成白色沉淀,向该溶液中加入氯化钡溶液,生成白色沉淀,可能含有硫酸钠或碳酸钠或两种都有,故C错误;
D、碳酸钠和硝酸反应会生成二氧化碳气体,所以向白色沉淀中加入足量稀硝酸,无现象,则白色固体中一定没有碳酸钠,故D正确.
故选:C.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
5.下列有关能源的叙述正确的是( )
| A. | 石油是一种可再生资源 | |
| B. | 大量使用化石能源会造成大气污染,因此应该停止化石能源的开采和利用 | |
| C. | 人类需要的能量都是由化学反应产生的 | |
| D. | 目前没有大量使用氢能源,是由于氢气的制取成本高,贮存困难 |
16.下列叙述正确的是( )
| A. | 氮气的化学性质不活泼,常用作保护气 | |
| B. | 酸雨的pH小于7,pH小于7的雨水一定是酸雨 | |
| C. | 催化剂能加快化学反应速率 | |
| D. | 溶液中有晶体析出,其溶质质量减小,所以溶质的质量分数一定减小 |
13.下列有关叙述正确的是( )
| A. | 原子核是由质子和中子构成的,所以所有原子的原子核都含有质子和中子 | |
| B. | 常见的铁合金有生铁和钢,其中钢的含碳量比生铁的高 | |
| C. | 石墨具有滑腻感,因此石墨可以做铅笔芯 | |
| D. | 喝了汽水会打嗝,因为温度升高,气体的溶解度减小 |
20.我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),促进了世界制碱技术的发展.下列有关说法正确的是( )
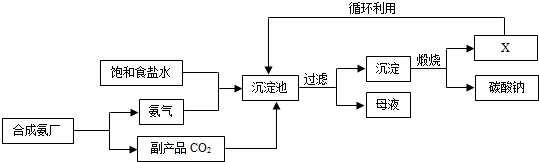

| A. | 沉淀池中的反应物共含有三种 | |
| B. | 过滤得到的“母液”中一定只含有两种溶质 | |
| C. | 图中X可能是氨气 | |
| D. | 通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀 |
17.茶叶中含有的茶氨酸(C7H14O3N2)可以降低血压、提高记忆力、保护神经细胞等.下列有关茶氨酸的说法中,正确的是( )
| A. | 一个茶氨酸分子中含有一个氮分子 | |
| B. | 茶氨酸属于有机高分子化合物 | |
| C. | 茶氨酸中碳元素与氢元素的质量比为6:1 | |
| D. | 茶氨酸中氢元素的质最分数最大 |
14.酸、碱、盐类物质在工农业生产中具有广泛应用.有关说法不正确的是( )
| A. | 将氯化铵与草木灰混合施用 | |
| B. | 从内陆盐湖中提取纯碱 | |
| C. | 用石灰乳与硫酸铜溶液配制波尔多液 | |
| D. | 高温煅烧石灰石制取生石灰 |
 稀有气体包括氦、氖、氩、氪、氙和氡六种气体,约占空气体积的0.94%.常温常压下,稀有气体都是无色无味,微溶于水,且熔点和沸点都很低.由于稀有气体元素原子的最外层电子排布是稳定结构,所以它们的化学性质非常稳定,但在一定条件下,氙气(Xe)可与氟气(F2)发生反应,生成四氟化氙(XeF4).工业上,制取稀有气体是通过将液态空气蒸馏,得到稀有气体的混合物,再用活性炭低温吸附法,将稀有气体分离开来.在焊接精密零件或镁、铝等活泼金属时,常用氩作保护气.氦气是除了氢气外的最轻气体,可以代替氢气应用在飞艇中,不会着火和发生爆炸.利用稀有气体通电时发出色彩绚丽的光芒,可制成霓虹灯.
稀有气体包括氦、氖、氩、氪、氙和氡六种气体,约占空气体积的0.94%.常温常压下,稀有气体都是无色无味,微溶于水,且熔点和沸点都很低.由于稀有气体元素原子的最外层电子排布是稳定结构,所以它们的化学性质非常稳定,但在一定条件下,氙气(Xe)可与氟气(F2)发生反应,生成四氟化氙(XeF4).工业上,制取稀有气体是通过将液态空气蒸馏,得到稀有气体的混合物,再用活性炭低温吸附法,将稀有气体分离开来.在焊接精密零件或镁、铝等活泼金属时,常用氩作保护气.氦气是除了氢气外的最轻气体,可以代替氢气应用在飞艇中,不会着火和发生爆炸.利用稀有气体通电时发出色彩绚丽的光芒,可制成霓虹灯.