题目内容
我国早在春秋战国时期,就开始生产和使用铁器。某化学小组到钢铁厂做社会调查,将不同质量的生铁样品(假定其中只含铁和碳两种单质)分别放入5只烧杯中,各加入189.2 g质量分数相同的稀硫酸进行实验,实验数据见下表:
| 烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ |
加入生铁样品 的质量/g | 3.0 | 6.0 | 9.0 | 12.4 | 14.0 |
充分反应后 生成气体 的质量/g | 0.1 | M | 0.3 | 0.4 | 0.4 |
试计算:
(1)表中M的值为________。
(2)烧杯④中完全反应后,所得溶液中溶质的质量是多少?(写出计算过程)
【答案】
(1)0.2?? (2)30.4 g(计算过程见解析)
【解析】本题以某化学小组到钢铁厂做社会调查,将不同质量的生铁样品与稀硫酸反应的数据为主题,考查化学方程式的计算。解题的关键有:(1)首先要推断出M的数值。比较烧杯①和烧杯③中的生铁样品及产生的气体可以知道,每3.0 g生铁样品与足量稀硫酸反应后能生成0.1 g氢气,所以可以判断M的值为0.2;(2)分析表中数据,明确哪组实验中铁样品和稀硫酸完全反应。比较烧杯③和烧杯④中数据可以知道,生铁的质量增加12.4 g-9.0 g=3.4 g,但是气体的质量只增加了0.1 g,结合(1)的分析可以判断稀硫酸已完全反应。(3)知道189.2 g稀硫酸可以消耗生铁的质量为12.0 g,此时,溶液中的溶质为硫酸亚铁,据此结合化学方程式来完成解答。
解:设生成硫酸亚铁的质量为y。
Fe+H2SO4=FeSO4+H2↑
???????? 152??? 2
????????? y??? 0.4 g
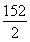 =
= 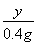
y= 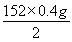 =30.4 g
=30.4 g
答:所得FeSO4溶液中溶质的质量为30.4 g

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
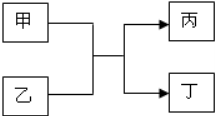 甲、乙、丙、丁是初中化学的常见物质,它们有如图的转化关系:
甲、乙、丙、丁是初中化学的常见物质,它们有如图的转化关系: