题目内容
制备硅半导体材料必须先得到高纯硅,三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法.生产过程示意如下:
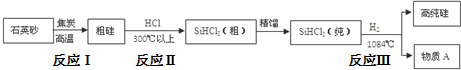
(1)石英砂的主要成分是二氧化硅和碳在高温的条件下反应生成硅和一种无色的可燃性气体,请写出反应Ⅰ的化学方程式 ;
(2)写出反应Ⅱ的化学方程式 .
(3)写出反应Ⅲ的化学方程式 .
(4)整个制备过程必须达到无水无氧.在H2还原SiHCl3过程中若混入O2,可能引起的后果是 .
(5)在生产过程中物质A可循环使用,A的化学式是 ;在生产过程中还有一种可循环使用的物质是 .

(1)石英砂的主要成分是二氧化硅和碳在高温的条件下反应生成硅和一种无色的可燃性气体,请写出反应Ⅰ的化学方程式
(2)写出反应Ⅱ的化学方程式
(3)写出反应Ⅲ的化学方程式
(4)整个制备过程必须达到无水无氧.在H2还原SiHCl3过程中若混入O2,可能引起的后果是
(5)在生产过程中物质A可循环使用,A的化学式是
考点:物质的相互转化和制备,书写化学方程式、文字表达式、电离方程式,氢气的化学性质与燃烧实验
专题:物质的制备
分析:分析制备高纯硅的主要方法和生产过程,根据题干中的反应写出有关的化学方程式;根据氢气与氧气反应的情况和Si与氧气反应的情况分析在H2还原SiHCl3过程中若混入O2可能引起的后果;根据生产过程分析可循环使用的物质.
解答:解:(1)二氧化硅和碳在高温的条件下反应生成硅和一种无色的可燃性气体,由质量守恒定律可知,此气体
为一氧化碳,反应的化学方程式是:2C+SiO2
Si+2CO↑.
(2)由反应的过程可知,反应Ⅱ是由粗硅制取三氯甲硅烷,反应的化学方程式是:Si+3HCl
SiHCl3+H2;
(3)由反应的过程可知,反应Ⅲ是由H2还原SiHCl3制备高纯度的硅,反应的方程式是:SiHCl3+H2
Si+3HCl;
(4)在H2还原SiHCl3过程中若混入O2,H2与O2在高温下容易爆炸,Si与O2生成氧化物,所以,可能引起的后果是硅被氧化得不到高纯硅,还会引起爆炸;
(5)在上述生产流程中由粗硅到三氯甲硅烷和由三氯甲硅烷到高纯硅是两个相反的过程,在生产过程中物质A可循环使用,A的化学式是HCl;在生产过程中还有一种可循环使用的物质是H2.
故答为:(1)2C+SiO2
Si+2CO↑;(2)Si+3HCl
SiHCl3+H2;(3)SiHCl3+H2
Si+3HCl;(4)硅被氧化得不到高纯硅,还会引起爆炸;(5)HCl,H2.
为一氧化碳,反应的化学方程式是:2C+SiO2
| ||
(2)由反应的过程可知,反应Ⅱ是由粗硅制取三氯甲硅烷,反应的化学方程式是:Si+3HCl
| ||
(3)由反应的过程可知,反应Ⅲ是由H2还原SiHCl3制备高纯度的硅,反应的方程式是:SiHCl3+H2
| ||
(4)在H2还原SiHCl3过程中若混入O2,H2与O2在高温下容易爆炸,Si与O2生成氧化物,所以,可能引起的后果是硅被氧化得不到高纯硅,还会引起爆炸;
(5)在上述生产流程中由粗硅到三氯甲硅烷和由三氯甲硅烷到高纯硅是两个相反的过程,在生产过程中物质A可循环使用,A的化学式是HCl;在生产过程中还有一种可循环使用的物质是H2.
故答为:(1)2C+SiO2
| ||
| ||
| ||
点评:此题主要是考查学生的综合分析能力,不但要求学生具备有关物质的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力

练习册系列答案
相关题目
下列符号既能表示一种元素,又能表示这种元素的一个原子,又能表示这种物质的是( )
| A、H | B、O | C、Cl | D、C |
如图是某化学反应的微观模型,“○”、“●”分别表示不同元素的原子,下列对图示模型理解正确的是( )
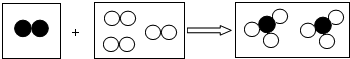

| A、该反应属于化合反应 |
| B、参加反应的两种物质分子个数之比为1:1 |
| C、反应物和生成物中共含有三种元素 |
| D、反应物和生成物中只有一种单质 |
除去下列物质中的杂质,所需药品(括号中的物质)选择不正确的是( )
| A、NaCl溶液中含有少量的Na2SO4[Ba(NO3)2溶液] |
| B、CO2中含有少量的水蒸气(浓硫酸) |
| C、NaOH溶液中含有少量的Na2CO3(石灰水) |
| D、铜粉中含有少量的氧化铜(稀盐酸) |
2011年3月日本发生海啸,灾民饮用水被严重污染,急需进行净化处理.下列净化水的单一操作中,净化程度最高的是( )
| A、蒸馏 | B、吸附沉淀 |
| C、过滤 | D、静置沉淀 |
下列几种说法,你认为正确的是( )
| A、碱类物质一定能使酚酞溶液变红色 |
| B、有盐和水生成的反应不一定是中和反应 |
| C、酸性溶液就是酸溶液 |
| D、能与碱反应生成盐和水的化合物一定是酸 |
物质在“潮湿空气”中发生变化主要与空气中某些气体有关,下列说法不正确的是( )
| A、钢铁生锈与氧气、水蒸气有关 |
| B、生石灰堆放久了变质与氧气、水蒸气有关 |
| C、铜器表面生成铜绿[Cu2(OH)2CO3]与氧气、二氧化碳、水蒸气有关 |
| D、氢氧化钠固体潮解、变质与水蒸气、二氧化碳有关 |