题目内容
4.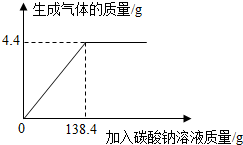 向一定质量、一定溶质质量分数的稀盐酸中逐滴加入某碳酸钠溶液.实验过程中,产生气体质量与加入碳酸钠溶液的质量关系如图所示,试计算:
向一定质量、一定溶质质量分数的稀盐酸中逐滴加入某碳酸钠溶液.实验过程中,产生气体质量与加入碳酸钠溶液的质量关系如图所示,试计算:(1)恰好完全反应时,生成气体的质量为4.4g;
(2)恰好完全反应时,所加碳酸钠溶液中Na2CO3的质量是多少?
(3)若恰好完全反应时所得溶液的溶质质量分数为5%,则稀盐酸的溶质质量分数是多少?
分析 (1)由图中数据可知恰好完全反应时生成CO2的质量;
(2)根据二氧化碳的质量,利用反应的化学方程式计算碳酸钠的质量,进一步可以计算两种物质恰好完全反应时所得溶液的溶质质量分数.
解答 解:
(1)恰好完全反应时生成CO2的质量为4.4g;
(2)设恰好完全反应时,所加碳酸钠溶液中Na2CO3的质量为x,碳酸钠完全反应生成氯化钠的质量为y,消耗稀盐酸的溶质质量为z
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
x z y 4.4g
$\frac{106}{x}=\frac{44}{4.4g}$
x=10.6g
$\frac{73}{z}=\frac{117}{y}=\frac{44}{4.4g}$
z=7.3g
y=11.7g
若恰好完全反应时所得溶液的质量=$\frac{11.7g}{5%}$=234g
稀盐酸的溶液质量=234g+4.4g-138.4g=100g
则稀盐酸的溶质质量分数是$\frac{7.3g}{100g}×$100%=7.3%
答案:
(1)4.4;
(2)恰好完全反应时,所加碳酸钠溶液中Na2CO3的质量是10.6g
(3)稀盐酸的溶质质量分数是7.3%.
点评 本题主要考查化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.本题较复杂,计算的知识点多,学生利用图象分析出二氧化碳的质量代入化学反应方程式计算是解答的突破口.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.对盐的组成叙述正确的是( )
| A. | 都含有原子团 | B. | 都含有金属元素 | ||
| C. | 都不含氢元素 | D. | 都含有非金属元素 |
12.如图是X、Y、Z三种液体的对应近似pH,下列判断不正确的是( )
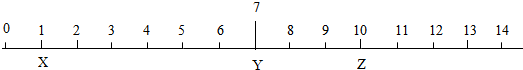
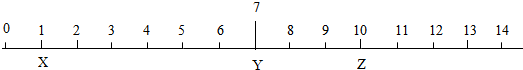
| A. | X显酸性 | B. | Y一定是水 | ||
| C. | Z可能是碳酸钠溶液 | D. | Z可使紫色石蕊试液变蓝 |
9.把少量的下列物质分别放入水中,充分搅拌,不能得到溶液的是( )
| A. | 食盐 | B. | 植物油 | C. | 蔗糖 | D. | 高锰酸钾 |
16.为了解决化石能源面临耗尽的问题,科学家正在开发新能源,下列不属于新能源的是( )
| A. | 天然气 | B. | 太阳能 | C. | 地热能 | D. | 潮汐能 |
14.下列变化属于化学变化的是( )
| A. | 蜡烛熔化 | B. | 铁水铸锅 | C. | 纸张燃烧 | D. | 海水晒盐 |