题目内容
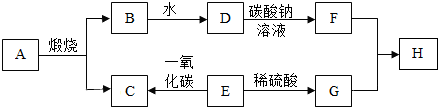
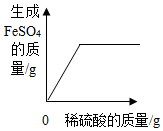
18.某工厂从硫酸铜废液中回收金属铜.将一定量的铁粉加入到硫酸铜废液中,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生,则滤渣中一定含有铜,一定不含有铁;滤液中一定含有的溶质是硫酸亚铁.分析 金属铁、铜的活动性由强到弱的顺序为:铁>铜,则向硫酸铜溶液中加入铁粉,铁粉与硫酸铜反应,置换出铜;向滤渣固体滴加稀盐酸,无气泡,说明加入的铁粉全部反应.
解答 解:加入铁粉与硫酸铜反应生成硫酸铜,若恰好完全反应,则滤液中不含硫酸铜,所以,滤液中一定含有硫亚铁;铁粉与硫酸铜反应,置换出铜,向滤渣固体滴加稀盐酸,无气泡,说明加入的铁粉全部反应,故滤渣中一定含有铜,一定不含有铁.
故答案为:铜;铁;硫酸亚铁.
点评 利用金属的活动性,判断反应的发生情况:滴加稀盐酸检验锌粉反应情况,无气泡,说明所加锌粉已完全反应.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
9.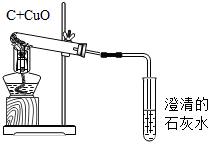 如图是木炭与氧化铜反应的实验装置图,下列说法错误的是( )
如图是木炭与氧化铜反应的实验装置图,下列说法错误的是( )
 如图是木炭与氧化铜反应的实验装置图,下列说法错误的是( )
如图是木炭与氧化铜反应的实验装置图,下列说法错误的是( )| A. | 给酒精灯加网罩,目的是使火焰集中并提高温度 | |
| B. | 实验过程中,可观察到澄清石灰水变浑浊 | |
| C. | 碳在反应中发生了氧化反应,表现出还原性 | |
| D. | 实验结束后,应先停止加热,再将导气管从澄清石灰水中撤出 |
6.下列有关金属及其合金的说法正确的是( )
| A. | 黄铜的硬度比铜的硬度小 | |
| B. | 不锈钢用于制作医疗器械 | |
| C. | 部分浸入食盐水中的铁钉不易生锈 | |
| D. | 防止金属腐蚀是保护金属资源的唯一途径 |
3.某同学用如图装置,进行有关碳及其氧化物的实验(图中夹持已略去),在完成气密性检査后加入药品,并已在装置中充满二氧化碳.
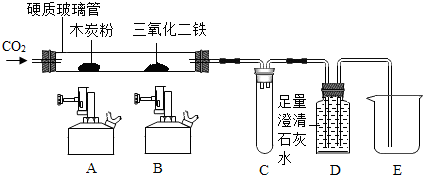
(1)填写表格中的空白内容:
(2)有同学认为该装罝需要添加尾气处理装置,你认为是否需要并说明理由不需要,未反应的CO进入D装置不会逸散到空气中..

(1)填写表格中的空白内容:
| 实验步骤 | 实验现象 | 实验分析 |
| ①缓缓通入CO2,点燃A处酒精喷灯,加热一段时间 | 木炭粉减少,D中有气泡产生、澄清石灰水变浑浊且石灰水沿右侧导气管进入E | 硬质玻璃管中发生反应的化学方程式为: C+CO2$\frac{\underline{\;高温\;}}{\;}$2C0 |
| ②点燃B处酒精喷灯,加热一段时间 | B处玻璃管内红色粉末变为黑色 | 以上实验说明一氧化碳具有还原性 |
| ③停止通入二氧化碳,熄灭A、B两处的火焰 | C中有D中液体进入 | / |
10.下列过程中主要发生物理变化的是( )
| A. | 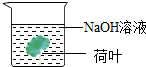 | B. | 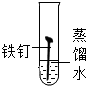 | C. | 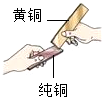 | D. | 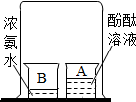 |
7.分类、类比是学习化学常用的方法.
(1)化学实验可按其主要目的分为:探究物质的性质、混合物的分离提纯,探究物质的含量等.因此应将下列实验中的B与C(填“A”或“C”或“D”)归为一类,依据是都属于混合物的分离.
(2)再反应C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO中,具有氧化性的反应物是二氧化碳.请写出一个两种化合物发生反应的化学方程式(其中一种化合物体现氧化性,另一种化合物体现还原性)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(1)化学实验可按其主要目的分为:探究物质的性质、混合物的分离提纯,探究物质的含量等.因此应将下列实验中的B与C(填“A”或“C”或“D”)归为一类,依据是都属于混合物的分离.
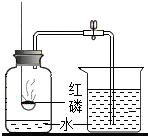 | 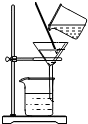 | 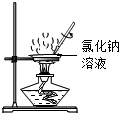 | 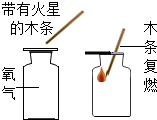 |
| A | B | C | D |
19.下列各组离子在水中能大量共存的是( )
| A. | Na+、H+、Cl-、CO32- | B. | Na+、K+、NO3-、Cl- | ||
| C. | H+、Na+、OH-、SO42- | D. | Ca2+、Na+、CO32-、NO3- |