题目内容
4.A、B、C、D、E、F都是初中化学中常见的化合物,其中B是酸,A、F是碱,它们之间可发生如下反应:①A+B→C+D ②C+F→A↓(红褐色)+Na2SO4 ③E+B→C+D
根据上述信息回答:
(1)写出有关物质的化学式:AFe(OH)3;BH2SO4.
(2)写出下列反应的化学方程式:
反应①2Fe(OH)3+3H2SO4═Fe2(SO4)3+6H2O;
反应②Fe2(SO4)3+6NaOH═2Fe(OH)3↓+3Na2SO4.
分析 根据题干叙述进行分析,③C+F→A↓(红褐色)+Na2SO4,A、F是碱,则推测A是氢氧化铁,F是氢氧化钠,C是硫酸铁;①A+B→C+D,因为C是硫酸铁、B是酸,则推测B是稀硫酸; ②E+B→C+D,B是稀硫酸,E是氢氧化铁,则D是水,据此解答即可.
解答 解:根据③C+F→A↓(红褐色)+Na2SO4,A、F是碱,则推测A是氢氧化铁,F是氢氧化钠,C是硫酸铁;①A+B→C+D,因为C是硫酸铁、B是酸,则推测B是稀硫酸; ②E+B→C+D,B是稀硫酸,E是氢氧化铁,则D是水,代入题干,推断合理;
(1)根据分析,物质A是氢氧化铁,B为稀硫酸,故其化学式分别为:Fe(OH)3;H2SO4.
(2)反应①中A是氢氧化铁,B为稀硫酸,则A+B→C+D的反应,即氢氧化铁与稀硫酸反应生成硫酸铁和水,反应的化学方程式为:2Fe(OH)3+3H2SO4═Fe2(SO4)3+6H2O.
反应②中C是硫酸铁,F是氢氧化钠,则C+F→A↓(红褐色)+Na2SO4的反应,即硫酸铁与氢氧化钠反应生成氢氧化铁沉淀和硫酸钠,其反应的化学方程式为:Fe2(SO4)3+6NaOH═2Fe(OH)3↓+3Na2SO4.
故答案为:
(1)Fe(OH)3; H2SO4.
(2)2Fe(OH)3+3H2SO4═Fe2(SO4)3+6H2O;
Fe2(SO4)3+6NaOH═2Fe(OH)3↓+3Na2SO4.
点评 本题考查了常见物质的推断题,完成此题,可以依据题干提供的信息结合物质的性质以及反应时的有关现象进行.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案
相关题目
5.下列变化中,不属于化学变化的是( )
| A. | 葡萄糖氧化 | B. | 将小麦加工成面粉 | ||
| C. | 用糯米酿酒 | D. | 蛋白质遇浓硝酸呈黄色 |
15.生活中的下列变化不属于化学变化的是( )
| A. | 苹果榨汁 | B. | 葡萄酿酒 | C. | 剩饭变馊 | D. | 铁器生锈 |
12.做完氢氧化钠与稀硫酸反应的实验后,化学小组的同学对自己实验后溶液中的溶质成分产生了兴趣,分别取自己实验后的溶液进行进一步探究,请回答:
【提出问题】溶液中的溶质是什么(忽略空气对溶液的影响)?
【作出猜想】猜想一:溶质只有Na2SO4
猜想二:溶质是Na2SO4和NaOH两种物质
猜想三:溶质是Na2SO4和硫酸(H2SO4)
【实验验证】
(1)小组同学先另取一瓶Na2SO4溶液,测定其其pH,测得pH=7.
(2)甲同学用酸碱指示剂,乙同学没有用酸碱指示剂,都验证了猜想二,请填表.
(3)丙同学设计了如下两个方案验证猜想三:
下列对上述两个方案的判断正确的是D(填序号).
A.只有方案①合理 B.只有方案②合理 C.两个方案都合理 D.两个方案都不合理
请你设计一个方案验证猜想三,但所选试剂不能是酸碱指示剂和盐溶液.
【提出问题】溶液中的溶质是什么(忽略空气对溶液的影响)?
【作出猜想】猜想一:溶质只有Na2SO4
猜想二:溶质是Na2SO4和NaOH两种物质
猜想三:溶质是Na2SO4和硫酸(H2SO4)
【实验验证】
(1)小组同学先另取一瓶Na2SO4溶液,测定其其pH,测得pH=7.
(2)甲同学用酸碱指示剂,乙同学没有用酸碱指示剂,都验证了猜想二,请填表.
| 实验操作 | 实验现象 | 实验结论 | |
| 甲同学 方案 | 取中和反应后的溶液少许于试管中,向试管中滴加几滴无色酚酞试液 | 溶液呈红色 | 猜想二成立 |
| 乙同学 方案 | 取中和反应后的溶液少许于试管中,向试管中滴加硫酸铜溶液 | 产生蓝色沉淀 | 猜想二成立 |
| 实验操作 | 实验现象 | 实验结论 | |
| 方案① | 取中和反应后的溶液少许于 试管中,向试管中滴加几滴 无色酚酞试液 | 溶液呈无色 | 猜想三 成立 |
| 方案② | 取中和反应后的溶液少许于 试管中,滴加几滴 BaCl2试液 | 产生白色沉淀 | 猜想三 成立 |
A.只有方案①合理 B.只有方案②合理 C.两个方案都合理 D.两个方案都不合理
请你设计一个方案验证猜想三,但所选试剂不能是酸碱指示剂和盐溶液.
| 实验方案 | 实验现象 | 有关的化学方程式 | 实验结论 |
| 取中和反应后的溶液少许于试管中,加入氧化铜固体 | 氧化铜溶解,溶液变蓝色 | CuO+H2SO4═CuSO4+H2O | 猜想三成立 |
9.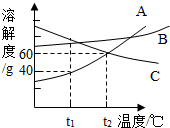 如图是A、B、C三种物质的溶解度曲线.下列说法不正确的是( )
如图是A、B、C三种物质的溶解度曲线.下列说法不正确的是( )
 如图是A、B、C三种物质的溶解度曲线.下列说法不正确的是( )
如图是A、B、C三种物质的溶解度曲线.下列说法不正确的是( )| A. | t2℃时,A和C的饱和溶液中溶质的质量分数相等 | |
| B. | t1℃时,100g水溶解了40gA就达到了饱和状态 | |
| C. | A的溶解度大于C的溶解度溶质的质量分数相等 | |
| D. | A和B的饱和溶液从t2℃降到t1℃时,溶液的溶质质量分数都变小 |
16.下列说法中正确的是( )
| A. | 氧气能够燃烧 | |
| B. | 空气的主要成分是氮气和氧气 | |
| C. | 金刚石、石墨都是天然存在的最硬物质 | |
| D. | 一氧化碳和二氧化碳都能将氧化铜还原为铜 |
13.【实验一】结合下列实验装置图回答问题
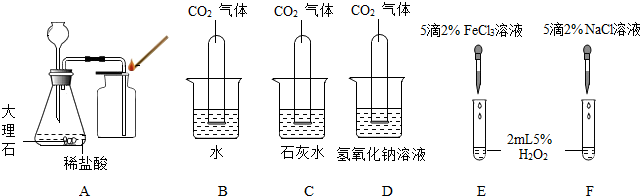
(1)用A图制取二氧化碳气体,反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O,若锥形瓶内的反应进行较长时间后,用燃着的火柴放在集气瓶口,火焰仍不熄灭,则是由于A装置存在缺陷,其缺陷为长颈漏斗未伸入液面,造成气体逸出;
(2)图B、C、D是探究二氧化碳化学性质的实验,C中发生反应的化学方程式是CO2+Ca(OH)2=CaCO3↓+H2O,,证明二氧化碳与氢氧化钠溶液发生反应的现象是C中有白色沉淀生成;
(3)图E和F是探究哪种离子能促进H2O2分解的实验,现象是:E中产生大量气泡,F中没有明显现象,则促进H2O2分解的离子符号是Fe3+.
【实验二】探究燃烧的条件
实验:下图的装置可用于探究燃烧的条件
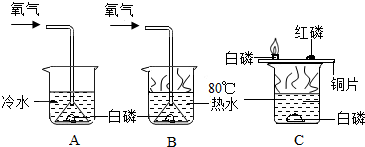
现象:①不通氧气时,A中白磷不燃烧
②不通氧气时,B中白磷不燃烧
③通氧气时,A中白磷不燃烧
④通氧气时,B中白磷燃烧
(1)证明可燃物燃烧,温度必须达到着火点的现象是③④(填序号);
(2)A、B组合与C装置相比的优点是C装置在密闭环境中进行,避免了P2O5对空气的污染.
【实验三】老师在课堂上说:“氢氧化钡与氢氧化钙化学性质相似”.化学兴趣小组的同学决定用氢氧化钡溶液来进行验证,他们做了以下实验.
结论:氢氧化钡的化学性质与氢氧化钙相似.
(1)写出实验三中发生反应的化学方程式Na2CO2+Ba(OH)2═BaCO3↓+2NaOH;
同学们将上述反应后的废液倒入烧杯中,过滤后,得到白色沉淀和红色滤液,他们决定对沉淀和滤液进行探究.
探究一:
【提出问题】沉淀能否与酸发生反应?
【实验探究】向沉淀中加入足量的稀硫酸,有气泡产生,白色固体不消失.
【实验结论】沉淀与酸不反应.
(2)有同学提出,根据“白色固体不消失”这一现象所得出的结论不严谨,理由是硫酸钡也是白色固体;
探究二:
【提出问题】滤液中除酚酞外,还有哪些溶质?
【作出猜想】Ⅰ.只有氢氧化钠Ⅱ.有氢氧化钠和碳酸钠Ⅲ.有氢氧化钠和氢氧化钡
【实验探究】
(3)有同学提出:实验四由于实验操作存在问题,导致结论不准确,该实验 操作上存在的问题是加入的稀盐酸的量太少,现象不明显;
【反思交流】
(4)小组同学经分析、讨论后发现,只用一种溶液做一次实验,就可以验证猜想,该溶液是稀硫酸;
(5)在废液中滴加稀盐酸至红色消失(填写实验现象)时,表示废液已呈中性.

(1)用A图制取二氧化碳气体,反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O,若锥形瓶内的反应进行较长时间后,用燃着的火柴放在集气瓶口,火焰仍不熄灭,则是由于A装置存在缺陷,其缺陷为长颈漏斗未伸入液面,造成气体逸出;
(2)图B、C、D是探究二氧化碳化学性质的实验,C中发生反应的化学方程式是CO2+Ca(OH)2=CaCO3↓+H2O,,证明二氧化碳与氢氧化钠溶液发生反应的现象是C中有白色沉淀生成;
(3)图E和F是探究哪种离子能促进H2O2分解的实验,现象是:E中产生大量气泡,F中没有明显现象,则促进H2O2分解的离子符号是Fe3+.
【实验二】探究燃烧的条件
实验:下图的装置可用于探究燃烧的条件

现象:①不通氧气时,A中白磷不燃烧
②不通氧气时,B中白磷不燃烧
③通氧气时,A中白磷不燃烧
④通氧气时,B中白磷燃烧
(1)证明可燃物燃烧,温度必须达到着火点的现象是③④(填序号);
(2)A、B组合与C装置相比的优点是C装置在密闭环境中进行,避免了P2O5对空气的污染.
【实验三】老师在课堂上说:“氢氧化钡与氢氧化钙化学性质相似”.化学兴趣小组的同学决定用氢氧化钡溶液来进行验证,他们做了以下实验.
| 序 号 | 操 作 | 现 象 | 结 论 |
| 实验一 | 向氢氧化钡溶液中滴入酚酞 | 溶液变红 | 氢氧化钡溶液呈碱性 |
| 实验二 | 向实验一的溶液中通入 适量的二氧化碳 | 产生白色沉淀,红色消失 | 氢氧化钡溶液能与 二氧化碳反应 |
| 实验三 | 另取氢氧化钡溶液,滴入 一定量的碳酸钠溶液 | 产生白色沉淀 | 氢氧化钡溶液能与 碳酸钠溶液反应 |
(1)写出实验三中发生反应的化学方程式Na2CO2+Ba(OH)2═BaCO3↓+2NaOH;
同学们将上述反应后的废液倒入烧杯中,过滤后,得到白色沉淀和红色滤液,他们决定对沉淀和滤液进行探究.
探究一:
【提出问题】沉淀能否与酸发生反应?
【实验探究】向沉淀中加入足量的稀硫酸,有气泡产生,白色固体不消失.
【实验结论】沉淀与酸不反应.
(2)有同学提出,根据“白色固体不消失”这一现象所得出的结论不严谨,理由是硫酸钡也是白色固体;
探究二:
【提出问题】滤液中除酚酞外,还有哪些溶质?
【作出猜想】Ⅰ.只有氢氧化钠Ⅱ.有氢氧化钠和碳酸钠Ⅲ.有氢氧化钠和氢氧化钡
【实验探究】
| 序号 | 操作 | 现象 | 结论 |
| 实验四 | 取滤液样品于试管中, 加入几滴稀盐酸 | 没有明显现象 | 猜想Ⅱ不成立 |
| 实验五 | 取滤液样品于试管中, 加入几滴碳酸钠溶液 | 有白色沉淀产生,红色不消失 | 猜想Ⅲ成立 |
【反思交流】
(4)小组同学经分析、讨论后发现,只用一种溶液做一次实验,就可以验证猜想,该溶液是稀硫酸;
(5)在废液中滴加稀盐酸至红色消失(填写实验现象)时,表示废液已呈中性.
14.图示中的呃“错误操作”与图下面“可能产生的后果”不一致的是( )
| A. | 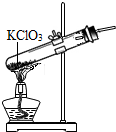 受热仪器破裂 | B. | 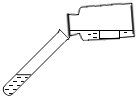 试剂外流 | C. | 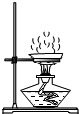 液体飞溅 | D. |  读数不正确 |