题目内容
14.我国科学家用滤纸和二氧化钛(TiO2)薄膜制作出一种新型“纳米纸”,又在纳米纸上“铺”一层“萘胺”(C10H9N)染料,制成一种试纸,用于检测食品中亚硝酸盐浓度的高低.下列说法不正确的是( )| A. | 二氧比钛属于氧化物 | |
| B. | 萘胺由三种元素组成 | |
| C. | 萘胺中氮元素的质量分数约为11.9% | |
| D. | 萘胺中碳、氢、氮三种元素的质量之比为120:9:14 |
分析 A.根据氧化物的概念来分析;
B.根据物质的组成来分析;
C.根据化合物中某元素质量分数公式进行分析;
D.根据元素质量比的计算方法来分析.
解答 解:A.二氧化钛是由钛元素和氧元素组成的化合物,属于氧化物,该选项说法正确;
B.由化学式可知,“萘胺”(C10H9N)是由碳、氢、氮三种元素组成的,该选项说法正确;
C.萘胺中氮元素的质量分数约为$\frac{14}{12×10+1×9+14}×100%$≈9.7%,故选项说法错误;
D.萘胺中碳元素、氢元素和氮元素的质量比为:(12×10):(1×9):(14×1)=120:9:14,该选项说法正确.
故选C.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算、有机物与化合物的特征等进行分析问题、解决问题的能力.

练习册系列答案
相关题目
9.下列物质按混合物、单质的顺序排列的是( )
| A. | 生理盐水、臭氧 | B. | 碳酸钙、金刚石 | C. | 冰水共存物、氮气 | D. | 空气、氧化镁 |
6.某实验小组的同学在做酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液中加入一定量的稀盐酸后,发现忘记了滴加酸碱指示剂,因此,他们停止滴加稀盐酸,并对烧杯中溶液的溶质成分进行探究.
【提出问题】该烧杯中溶液的溶质是什么?
【猜想与假设】猜想一:只有CaCl2;
猜想二:CaCl2和HCl;
猜想三:含有CaCl2、Ca(OH)2;
猜想四:含有CaCl2、Ca(OH)2、HCl.
同学们讨论后一致认为猜想四不合理,理由是稀盐酸与氢氧化钙在溶液中不能共存.
【查阅资料】氯化钙溶液呈中性
【进行实验】同学们设计可如下不同的实验方案,证明猜想二是成立的.请你帮他们填写有关实验步骤或实验现象.
【反思交流】
要使烧杯内溶液的溶质只含CaCl2,需要除去杂质,其中的一种方法是向烧杯中加入过量的碳酸钙,然后过滤,该除杂原理用化学方程式表示为CaCO3+2HCl=CaCl2+H2O+CO2↑.
【提出问题】该烧杯中溶液的溶质是什么?
【猜想与假设】猜想一:只有CaCl2;
猜想二:CaCl2和HCl;
猜想三:含有CaCl2、Ca(OH)2;
猜想四:含有CaCl2、Ca(OH)2、HCl.
同学们讨论后一致认为猜想四不合理,理由是稀盐酸与氢氧化钙在溶液中不能共存.
【查阅资料】氯化钙溶液呈中性
【进行实验】同学们设计可如下不同的实验方案,证明猜想二是成立的.请你帮他们填写有关实验步骤或实验现象.
| 方案 | 实验步骤 | 实验现象 |
| 方案一 | 取少量溶液于试管中,滴加紫色石蕊溶液 | 紫色石蕊溶液变红色 |
| 方案二 | 取少量氧化铜粉末于试管中,加入一定量的烧杯中的溶液 | 黑色粉末逐渐溶解,溶液变蓝色 |
要使烧杯内溶液的溶质只含CaCl2,需要除去杂质,其中的一种方法是向烧杯中加入过量的碳酸钙,然后过滤,该除杂原理用化学方程式表示为CaCO3+2HCl=CaCl2+H2O+CO2↑.
3.在化学方程式2XY+Y2=2Z中Z的化学式是( )
| A. | XY | B. | XY2 | C. | X2Y | D. | XY3 |
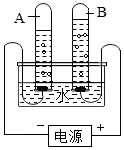 水是生命之源,它与我们的生活密切相关.
水是生命之源,它与我们的生活密切相关.