题目内容
4.生石灰是一种传统的建筑材料,俗称“石灰”.工业上通过在石灰窑中煅烧石灰石制得“石灰”,其反应原理是CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.(用化学方程式表示)某兴趣小组的同学对某地刚出窑的“石灰”的成分进行探究.
【提出问题】刚出窑的“石灰”有哪些成分?
【猜 想】Ⅰ.只有氧化钙Ⅱ.只有碳酸钙Ⅲ.既有氧化钙也有碳酸钙
【实验探究】
(1)晓明同学从样品中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物.据此晓明认为试管中的固体为碳酸钙,即猜想Ⅱ成立.晓红同学认为上述实验不足以证明猜想Ⅱ成立,其理由是沉淀也可能是未溶解的氢氧化钙.
(2)晓红同学从样品中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生.晓红同学据此认为试管中的固体只有氧化钙,即猜想Ⅰ成立.晓琳同学认为乙的实验不足以证明猜想Ⅰ成立,理由是滴加的稀盐酸不足量.
(3)晓琳同学认为还可以利用其他的方法判断是否有氧化钙,她用水、酚酞试液和稀盐酸证明了猜想Ⅲ成立,请完成她的实验报告.
| 实验步骤及现象 | 实验结论 |
| ①取少量剩余固体于试管中,加水振荡,试管外壁发烫,滤,取滤液滴加无色酚酞溶液,溶液变红 ②取滤渣滴加足量的稀盐酸,有气泡产生 | 猜想Ⅲ成立 |
温度,下列说法中正确的是C
A、溶剂质量不变 B、溶质质量增加 C、溶液浓度不变 D、溶解度增大
【思考】使用“石灰”的建筑工地上常有一个大的石灰池,使用“石灰”时,先将生石灰倒入池内水中,一段时间后,再取用其中的石灰浆使用.长期使用的石灰池内壁会逐渐增厚,其主要原因是Ca(OH)2+CO2=CaCO3↓+H2O.(用化学方程式表示)
分析 根据物质的性质进行分析,碳酸钙高温能分解生成氧化钙和二氧化碳,氧化钙能与水反应生成氢氧化钙,氢氧化钙是微溶于水的物质,其水溶液呈碱性,碳酸钙能与盐酸反应生成二氧化碳气体.虽然生石灰遇水会放出大量热而使饱和溶液温度升高,但题中明确“恢复到原来的温度”,因此在分析本问题时不需要考虑温度对溶液的影响;由于氧化钙能与水发生反应生成氢氧化钙,易被误解为增加了溶液中的溶质,其实,由于氧化钙反应消耗了饱和溶液中的水,而使饱和溶液因减少溶剂水而析出固体,饱和溶液的溶质、溶剂质量同时减少,溶液仍为饱和溶液.
解答 解:石灰石的主要成分是碳酸钙,碳酸钙在高温的条件下生成氧化钙和二氧化碳,方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
实验探究】(1)取一定量的剩余固体于试管中,加入一定量的水振荡,有白色不溶物不足以说明只有碳酸钙,因为氧化钙与水反应生成的氢氧化钙微溶于水,也是白色沉淀;
(2)取一定量的剩余固体于试管中,加入一定量的水,触摸试管外壁感觉发热,继续向试管中加入几滴稀盐酸,没有气泡产生,说明有氧化钙,氧化钙与水反应生成氢氧化钙,不能说明猜想Ⅲ成立,原因是即使有碳酸钙,加入的少量稀盐酸先消耗氢氧化钙,也不会出现气泡;
(3)利用水、无色酚酞溶液证明氧化钙与水反应生成氢氧化钙,用稀盐酸证明碳酸钙存在;步骤如下:
| 实验步骤及现象 | 实验结论 |
| ①取少量剩余固体于试管中,加水振荡,试管外壁发烫,过滤,取滤液滴加无色酚酞溶液,溶液变红 ②取滤渣滴加足量的稀盐酸,有气泡产生 | 猜想Ⅲ成立 |
B、由于氧化钙与饱和溶液中的水发生反应而使溶液因此减少了水,饱和溶液的溶剂减少会造成溶质析出;溶液的溶质、溶剂都在减少,故B错误;
C、饱和溶液随溶剂水的减少,溶质相应析出,变化后的溶液仍为饱和溶液,且溶液温度没有改变,根据相同温度下的同种溶质的饱和溶液的溶质质量分数相同,饱和溶液的溶质质量分数不变,故C正确;
D、固体物质的溶解度只受温度的影响,由于溶液的温度不变,因此,溶质的溶解度也不变,故D错误;
故选:C.
【思考】长期使用的石灰池内壁会逐渐增厚,其主要原因是:氢氧化钙吸收空气中的二氧化碳形成难溶的碳酸钙.
故答案为:
CaCO3$\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑;
【实验探究】
(1)沉淀也可能是未溶解的氢氧化钙;
(2)滴加的稀盐酸不足量;
(3)
| 实验步骤及现象 | 实验结论 |
| ①取少量剩余固体于试管中,加水振荡,试管外壁发烫,过滤,取滤液滴加无色酚酞溶液,溶液变红 ②取滤渣滴加足量的稀盐酸,有气泡产生 | 猜想Ⅲ成立 |
【思考】Ca(OH)2+CO2=CaCO3↓+H2O.
点评 本题考查了物质变质成分的探究,完成此题,可以依据已有的物质的性质进行.要求同学们熟练掌握常见物质的性质,以便灵活应用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.化学兴趣小组的同学发现,上个月做实验用的氢氧化钠溶液忘记了盖瓶盖.对于该溶液是否变质,小组内小明同学认为有两种可能:
猜想1:该溶液没有变质 猜想2:该溶液全部变质
(1)小组同学讨论后认为还有一种可能,请你补充出猜想3:该溶液部分变质.
(2)为了验证猜想3,小红同学设计了如下实验方案,请你帮他完成实验报告的填写
(3)探究启示:氢氧化钠必须保存.
猜想1:该溶液没有变质 猜想2:该溶液全部变质
(1)小组同学讨论后认为还有一种可能,请你补充出猜想3:该溶液部分变质.
(2)为了验证猜想3,小红同学设计了如下实验方案,请你帮他完成实验报告的填写
| 实验步骤 | 实验现象 | 结论 |
| 1.取样,过滤 | 产生白色沉淀 | 猜想3成立 |
| 2.向上述滤液中滴加溶液 | 酚酞溶液变红 |
17.下列实验操作中,错误的是( )
| A. |  滴加液体 | B. | 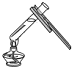 加热液体 | C. |  闻气体气味 | D. | 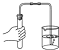 检查气密性 |
9.已知有些难溶物能溶于稀盐酸、稀硝酸,如:碳酸钙、碳酸钡等,有些难溶物不能溶于稀盐酸、稀硝酸,如:硫酸钡、氯化银等.现有一包固体粉末,可能由CaCO3、Na2SO4、KNO3、CuSO4、BaCl2中的一种或几种组成,做实验得以下结果:
(1)将此固体粉末加到水中,得到白色沉淀,且上层清液为无色;
(2)该白色沉淀部分溶予稀硝酸,并有无色气体产生.据此实验,得出的下列判断中正确的是( )
(1)将此固体粉末加到水中,得到白色沉淀,且上层清液为无色;
(2)该白色沉淀部分溶予稀硝酸,并有无色气体产生.据此实验,得出的下列判断中正确的是( )
| A. | 粉末中一定含有CaCO3、Na2SO4、BaCl2 | |
| B. | 该粉末中一定不含有KNO3、CuSO4 | |
| C. | 该粉末的组成中可能含有Na2SO4、KNO3 | |
| D. | 该粉末中一定含有Na2SO4、KNO3、BaCl2 |
13.第6000万种已知结构的新物质M化学式为C19H15N4FSO2.下列说法错误的是( )
| A. | M由六种元素组成,属于化合物 | B. | M的相对分子质量是42 | ||
| C. | M中氮氧原子个数比为2:1 | D. | 化学正在加快发展 |