题目内容
1.某物质R在氧的作用下发生反应:2R+2H2O+7O2═2FeSO4+2H2SO4,则R的化学式是( )| A. | FeS | B. | Fe2S3 | C. | FeO | D. | FeS2 |
分析 由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断反应物R的化学式.
解答 解:由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式2R+2H2O+7O2═2FeSO4+2H2SO4,反应前铁、硫、氧、氢原子个数分别为0、0、16、4,反应后的生成物中铁、硫、氧、氢原子个数分别为2、4、16、4,根据反应前后原子种类、数目不变,则2R分子中含有2个铁原子和4个氧原子,则每个R分子由1个铁原子和2个硫原子构成,则物质R的化学式为FeS2.
故选:D.
点评 本题难度不大,掌握利用化学反应前后原子守恒来确定物质的化学式的方法是正确解答此类题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.现代社会的生产和生活要消耗大量能量,下列活动中,通过化学反应提供能量的是( )
| A. |  发射航天飞机 | B. |  水力发电 | C. |  太阳能供热 | D. |  风力发电 |
10.下列关于空气的说法不正确的是( )
| A. | 空气属于混合物 | |
| B. | 空气中氧气的含量最多 | |
| C. | 红磷在空气中燃烧产生大量白烟 | |
| D. | 工业上常采用分离液态空气的方法制氧气 |
11.已知镁在氧气中燃烧生成氧化镁,要让6g镁条完全燃烧,需要氧气的质量是( )
| A. | 4g | B. | 1g | C. | 1.5g | D. | 无法计算 |
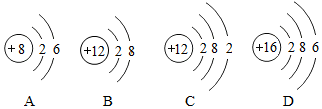 如图为4种粒子的结构示意图,完成以下空白,其中BC属于同种元素(填序号),其中化学性质相似的元素有AD.(填序号)
如图为4种粒子的结构示意图,完成以下空白,其中BC属于同种元素(填序号),其中化学性质相似的元素有AD.(填序号)