题目内容
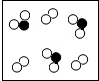
12. 如图所示电解水实验,回答下列问题:
如图所示电解水实验,回答下列问题:(1)A端电极为正极(填“正”或“负”).
(2)该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
分析 (1)根据电解水的实验结论:正氧负氢、氢二氧一,进行分析解答.
(2)电解水生成氢气和氧气,写出反应的化学方程式即可.
解答 解:(1)由电解水的实验结论:正氧负氢、氢二氧一,与A端相连的试管内产生的气体少,故A端电极为正极.
(2)电解水生成氢气和氧气,反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
故答案为:(1)正;(2)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
点评 本题难度不大,掌握电解水的实验结论(正氧负氢、氢二氧一)、化学方程式的书写方法是正确解答本题的关键.

练习册系列答案
相关题目
2.对以下三个化学反应的分析正确的是( )
C+O2$\stackrel{点燃}{→}$CO2 4P+5O2$\stackrel{点燃}{→}$2P2O5 CH4+O2$\stackrel{点燃}{→}$CO2+H2O.
C+O2$\stackrel{点燃}{→}$CO2 4P+5O2$\stackrel{点燃}{→}$2P2O5 CH4+O2$\stackrel{点燃}{→}$CO2+H2O.
| A. | 都属于化合反应 | B. | 反应温度都需达到着火点 | ||
| C. | 生成物均是气体 | D. | 反应时均产生蓝色火焰 |
3. 如图为地壳中元素含量分布图,其中能代表铝元素的是( )
如图为地壳中元素含量分布图,其中能代表铝元素的是( )
 如图为地壳中元素含量分布图,其中能代表铝元素的是( )
如图为地壳中元素含量分布图,其中能代表铝元素的是( )| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
20.氧化物AmOn中,A的化合价为( )
| A. | +2n | B. | +2m | C. | +$\frac{2n}{m}$ | D. | +$\frac{2m}{n}$ |
17.实验小组同学通过以下实验研究可燃物燃烧的条件.
已知:白磷的着火点是40℃,红磷的着火点是240℃.
(1)氧化钙与水反应的化学方程式为CaO+H2O═Ca(OH)2.
(2)此实验研究的可燃物的燃烧条件是达到可燃物的着火点.
已知:白磷的着火点是40℃,红磷的着火点是240℃.
| 实验装置 | 实验过程 | 实验现象 |
 | ①取一烧杯,加入适量的生石灰,再分别取少量白磷、红磷放在烧杯上的铜片上. ②向烧杯中加入一定量的冷水. | 一会儿白磷发生燃烧,红磷不燃烧. |
(2)此实验研究的可燃物的燃烧条件是达到可燃物的着火点.