题目内容
根据如图6种微粒结构图回答问题.
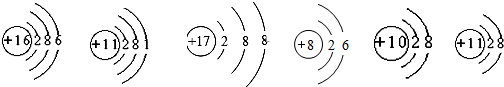
① ② .③ ④ ⑤ ⑥ ;
(1)填写各粒子对应的符号.
(2)能形成氯化钠的是 (填序号).
(3)属于阳离子的是 (填序号).
(4)已知微粒 ③的相对原子质量是36,则该原子核中的中子数是 .
(5)⑥的元素在周期表中的第 周期.
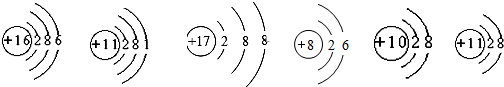
①
(1)填写各粒子对应的符号.
(2)能形成氯化钠的是
(3)属于阳离子的是
(4)已知微粒 ③的相对原子质量是36,则该原子核中的中子数是
(5)⑥的元素在周期表中的第
考点:原子结构示意图与离子结构示意图
专题:化学用语和质量守恒定律
分析:(1)根据元素符号的书写要求正确书写;
(2)根据氯化钠是钠离子和氯离子构成的;
(3)根据阳离子中:质子数>电子数分析解答;
(4)根据相对原子质量=质子数+中子数;
(5)根据周期数等于电子层数;
(2)根据氯化钠是钠离子和氯离子构成的;
(3)根据阳离子中:质子数>电子数分析解答;
(4)根据相对原子质量=质子数+中子数;
(5)根据周期数等于电子层数;
解答:解:(1)根据质子数决定元素种类,可知①为硫,②为钠,③为氯离子,④为氧,⑤为氖,⑥钠离子;
(2)氯化钠是钠离子和氯离子构成的;
(3)⑥中的质子数=11>电子数=10为阳离子;
(4)相对原子质量=质子数+中子数;该原子核中的中子数=36-17=19;
(5)周期数等于电子层数,⑥的元素有三个电子层,故再第三周期
答案:(1)①S;②Na;③Cl-;④O;⑤Ne;⑥Na+.
(2)③⑥;
(3)⑥;
(4)19;
(5)三.
(2)氯化钠是钠离子和氯离子构成的;
(3)⑥中的质子数=11>电子数=10为阳离子;
(4)相对原子质量=质子数+中子数;该原子核中的中子数=36-17=19;
(5)周期数等于电子层数,⑥的元素有三个电子层,故再第三周期
答案:(1)①S;②Na;③Cl-;④O;⑤Ne;⑥Na+.
(2)③⑥;
(3)⑥;
(4)19;
(5)三.
点评:本题考查学生根据微粒结构示意图及核电荷数、质子数与核外电子数的关系辨别微粒种类方法的掌握与应用的能力.

练习册系列答案
相关题目
下列对于化学式“CO2”的认识中,不正确的是( )
| A、表示二氧化碳这种物质 |
| B、表示一个二氧化碳分子 |
| C、表示二氧化碳是由氧原子和碳原子构成的 |
| D、表示二氧化碳是由氧元素和碳元素组成的 |
请从“氧气、氮气、二氧化碳、水蒸气、稀有气体、二氧化硫”等物质中,按要求将相应的物质填在题中的空白处.
(1)属于空气污染物的气体是 ;
(2)用于制造霓虹灯的是 ;
(3)用于填充食品包装以防腐的是 .
(1)属于空气污染物的气体是
(2)用于制造霓虹灯的是
(3)用于填充食品包装以防腐的是
下列粒子结构示意图中,表示阳离子的是( )
A、 |
B、 |
C、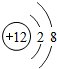 |
D、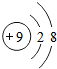 |
 根据下列每小题提出的问题填空.
根据下列每小题提出的问题填空.