题目内容
3.某兴趣小组对碱式碳酸铜的分解产物进行探究.【查阅资料】
①碱式碳酸铜受热分解的化学方程式为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑;
②白色的无水硫酸铜遇水会变成蓝色;
③CO还原CuO的实验过程中,固体产物可能有Cu2O(氧化亚铜,红色固体)、铜.
【实验验证】
验证碱式碳酸铜的分解产物,可选装置如下图所示.

(1)上图装置A中盛放的试剂名称是澄清石灰水.
(2)甲同学将装置按B→C→A(填字母,且每套装置限用一次)顺序组合进行实验,验证出碱式碳酸铜的分解产物中有二氧化碳和水.
(3)B装置中粉末完全变黑后,乙同学为确认该黑色粉末是氧化铜而不是碳粉,设计如下实验,请完成下表:
| 实验步骤 | 观察到的现象 | 获得结论 | 有关反应的化学方程式 |
| 取少量黑色粉末于试管中,向其中加入足量的稀硫酸,震荡 | 固体溶解,溶液变成蓝色 | 黑色粉末均为氧化铜 | CuO+H2SO4=CuSO4+H2O |
丙同学利用上述实验后的B装置(包括其中药品),探究CO还原CuO所得固体产物的成分,实验装置如图:

(1)实验过程:打开K,缓缓通入CO气体,一段时间后加热.当黑色固体全部变红后停止加热,继续通入CO气体直至玻璃管冷却.
(2)实验数据
| 反应前 | 反应后 |
| 玻璃管和内盛氧化铜粉末的总质量为62.0g | 玻璃管和内盛红色粉末的总质量为61.7 |
| 玻璃管的总质量为60.0g | |
(4)表达交流:下列有关该实验的说法正确的是BC.
A.该实验最好在通风橱中进行
B.先通入一会CO再加热是为了排净装置中的空气
C.装置图中虚线框内的装置既能吸收二氧化碳,又能收集一氧化碳
D.排入到烧杯中的溶液可能显碱性,也可能显中性.
分析 二氧化碳能使澄清石灰水变浑浊;
氧化铜和稀硫酸反应生成硫酸铜和水;
一氧化碳和氧化铜反应的过程中,根据反应前后玻璃管中的固体质量差可以计算判断固体组成;
二氧化碳和氢氧化钠反应生成碳酸钠和水,一氧化碳不能和氢氧化钠反应,不溶于水.
解答 解:【实验验证】
(1)上图装置A中盛放的试剂名称是澄清石灰水,目的是为了检验生成物中是否含有二氧化碳.
故填:澄清石灰水.
(2)甲同学将装置按B→C→A顺序组合进行实验,验证出碱式碳酸铜的分解产物中有二氧化碳和水.
故填:B→C→A.
(3)实验步骤:取少量黑色粉末于试管中,向其中加入足量的稀硫酸,震荡;
实验现象:固体溶解,溶液变成蓝色;
实验结论:黑色粉末为氧化铜;
氧化铜和稀硫酸反应的化学方程式为:CuO+H2SO4=CuSO4+H2O.
【拓展探究】
(3)如果玻璃管中的固体是铜,则铜的质量为:2.0g×$\frac{64}{80}$×100%=1.6g,而玻璃管中的固体质量为:62.0g-61.7g=0.3g,因此红色固体粉末为铜和氧化铜.
故填:铜和氧化铜.
(4)A.该实验对一氧化碳进行了收集,因此不需要在通风橱中进行;
B.先通入一会CO再加热是为了排净装置中的空气;
C.装置图中虚线框内的装置既能吸收二氧化碳,又能收集一氧化碳;
D.排入到烧杯中的溶液,无论是氢氧化钠溶液,还是碳酸钠溶液,还是氢氧化钠和碳酸钠的混合溶液,都显碱性.
故填:BC.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
14.下列变化属于化学变化的是( )
| A. | 冰雪融化 | B. | 榨取果汁 | C. | 火药爆炸 | D. | 液化空气 |
11.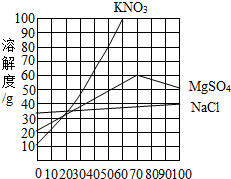 如图是三种物质的溶解度曲线.下列说法错误的是( )
如图是三种物质的溶解度曲线.下列说法错误的是( )
 如图是三种物质的溶解度曲线.下列说法错误的是( )
如图是三种物质的溶解度曲线.下列说法错误的是( )| A. | 升高温度,可以使三种物质的溶解度增大 | |
| B. | 降低温度.可以除去饱和KN03溶液中含有的少量NaCl | |
| C. | 50℃时,三种物质的溶解度由大到小的顺序是:KN03>MS04>NaCl | |
| D. | 50℃时,三种饱和溶液降温至10℃,所得溶液溶质的质量分数由大到小的顺序是:NaCl>MgSO4>KNO3 |
18. 如图所示的一组实验可用于研究燃烧条件.下列说法中正确的是( )
如图所示的一组实验可用于研究燃烧条件.下列说法中正确的是( )
 如图所示的一组实验可用于研究燃烧条件.下列说法中正确的是( )
如图所示的一组实验可用于研究燃烧条件.下列说法中正确的是( )| A. | 图1实验说明红磷的着火点比白磷的高 | |
| B. | 图1中水下白磷未燃烧是由于温度没有达到白磷的着火点 | |
| C. | 图2中水下白磷通氧气后能观察到燃烧现象 | |
| D. | 若将图2中白磷换成红磷,也能观察到燃烧现象 |
8.做木炭在氧气中燃烧的实验时,实验现象不明显,原因可能是( )
| A. | 用向下排空气法收集氧气 | |
| B. | 将集满氧气的集气瓶正放在桌面上 | |
| C. | 收集满氧气后,在水面下用玻璃片盖住瓶口移出水槽 | |
| D. | 收集氧气时,观察到导管口气泡连续均匀放出时开始收集 |
 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.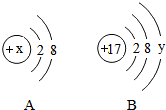 如图A、B分别是某微粒的结构示意图,回答下列问题:
如图A、B分别是某微粒的结构示意图,回答下列问题: