题目内容
(1)下列物质中,属于纯净物的是 (填写序号,下同),属于化合物的是 .
①液态氧 ②蒸馏水 ③干冰 ④天然气 ⑤过磷酸钙
(2)用离子符号表示:①三个钙离子 ; ②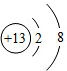 表示的是 .
表示的是 .
(3)用化学方程式解释:盐酸可以除去铁制品表面的铁锈(Fe2O3) .该反应的基本反应类型是 .
①液态氧 ②蒸馏水 ③干冰 ④天然气 ⑤过磷酸钙
(2)用离子符号表示:①三个钙离子
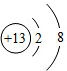 表示的是
表示的是(3)用化学方程式解释:盐酸可以除去铁制品表面的铁锈(Fe2O3)
考点:纯净物和混合物的判别,单质和化合物的判别,原子结构示意图与离子结构示意图,化学符号及其周围数字的意义,反应类型的判定,书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律,物质的分类
分析:(1)纯净物是由一种物质组成的物质.混合物是由多种物质组成的物质.单质是由同种元素组成的纯净物.化合物是由不同种元素组成的纯净物.
(2)元素符号前面的数字表示微粒个数,在元素符号右上角的数字表示电荷数,“+”表示正电荷;
(3)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
(2)元素符号前面的数字表示微粒个数,在元素符号右上角的数字表示电荷数,“+”表示正电荷;
(3)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答:解:(1)天然气的主要成分是甲烷,属于混合物.过磷酸钙中含有磷酸二氢钙和硫酸钙,属于混合物;①液态氧、②蒸馏水、③干冰都是由一种物质组成的,都属于纯净物.蒸馏水、干冰都是由不同种元素组成的纯净物,都属于化合物;
(2)镁的元素符号为Mg,元素符号前面的数字表示微粒个数,在元素符号右上角的数字表示电荷数,“+”表示正电荷,则三个镁离子可用3Mg2+表示;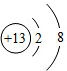 的核内质子数大于核外电子数,因此表示的是铝离子;
的核内质子数大于核外电子数,因此表示的是铝离子;
(3)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O;该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应.
故填:(1)①②③;②③;(2)3Ca2+;Al3+;(3)Fe2O3+6HCl═2FeCl3+3H2O;复分解反应.
(2)镁的元素符号为Mg,元素符号前面的数字表示微粒个数,在元素符号右上角的数字表示电荷数,“+”表示正电荷,则三个镁离子可用3Mg2+表示;
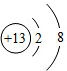 的核内质子数大于核外电子数,因此表示的是铝离子;
的核内质子数大于核外电子数,因此表示的是铝离子;(3)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O;该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应.
故填:(1)①②③;②③;(2)3Ca2+;Al3+;(3)Fe2O3+6HCl═2FeCl3+3H2O;复分解反应.
点评:化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
下列是一些物质的自我介绍,其中介绍了自己化学性质的是( )
| A、铜:我能导电 |
| B、氢气:我最轻 |
| C、氧气:液态时,我是淡蓝色 |
| D、碳酸氢铵:我贪凉,受热会分解 |
化学知识中有很多的“相等”.请你判断下列说法中不正确的是( )
| A、溶液稀释前后,溶质的质量相等 |
| B、化合物中元素化合价的正价总数与负价总数的数值相等 |
| C、50mL的水和50mL的酒精混合,所得溶液的体积等于100mL |
| D、氢氧化钠溶液和稀硫酸混合后,所得溶液的质量与反应前溶液的总质量相等 |
在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识错误的是( )
| 物质 | M | N | Q | P |
| 反应前质量(g) | 18 | 1 | 2 | 32 |
| 反应后质量(g) | X | 26 | 2 | 12 |
| A、该反应的反应类型是化合反应 |
| B、反应后物质M的质量为5 g |
| C、反应中N、P的质量比为5:4 |
| D、物质Q可能是该反应的催化剂 |
若想称取5.6g食盐粉末,称量过程中指针偏向右面,此时应该(其他操作均正确)( )
| A、继续添加食盐 |
| B、取出少量食盐放回试剂瓶 |
| C、取出少量食盐放到指定容器 |
| D、向外调节平衡螺母 |
发射“神舟十号”飞船的“长征二号F”运载火箭在升空时将会发生下列变化,其中属于化学变化的是( )
| A、火箭点火 |
| B、导流槽内的水受热汽化 |
| C、隔热材料脱落 |
| D、整流罩脱落 |