题目内容
4.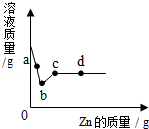 向一定量的硝酸银、硝酸铜和硝酸镁的混合溶液中加入Zn,溶液质量与Zn的质量关系如图所示.
向一定量的硝酸银、硝酸铜和硝酸镁的混合溶液中加入Zn,溶液质量与Zn的质量关系如图所示.①写出b→c段发生反应的化学方程式Zn+CuSO4=ZnSO4+Cu;
②b点对应的溶液中所含的金属离子有Mg2+、Zn2+、Cu2+.
分析 根据四种金属的活动性顺序是:镁、锌、铜、银,所以向一定量的硝酸银、硝酸铜和硝酸镁的混合溶液中加入Zn,锌会先与硝酸银反应,然后再与硝酸铜反应,a→b溶液质量减小,发生的反应是锌和硝酸银反应生成硝酸锌和银,溶液质量逐渐减小,b→c段发生的反应是锌和硝酸铜反应生成硝酸锌和铜进行分析.
解答 解:四种金属的活动性顺序是:镁、锌、铜、银,所以向一定量的硝酸银、硝酸铜和硝酸镁的混合溶液中加入Zn,锌会先与硝酸银反应,然后再与硝酸铜反应,a→b溶液质量减小,发生的反应是锌和硝酸银反应生成硝酸锌和银,溶液质量逐渐减小,b→c段发生的反应是锌和硝酸铜反应生成硝酸锌和铜,所以
①b→c段发生的反应是,锌和硝酸铜反应生成硝酸锌和铜,化学方程式为:Zn+CuSO4=ZnSO4+Cu;
②b点对应的溶液中所含的金属离子有Mg2+、Zn2+、Cu2+.
故答案为:①Zn+CuSO4=ZnSO4+Cu;
②Mg2+、Zn2+、Cu2+.
点评 活动性强的金属放入活动性弱的金属的混合盐溶液中,活动性强的金属会先把活动性最弱的金属从其盐溶液中置换出来,然后再置换活动性较弱的金属.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.小文同学在学习“生活中常见盐”时,对碳酸钠溶液与氢氧化钙溶液反应后所得滤液成分产生探究的兴趣,请你和他一起进行如下探究:
【提出问题】滤液中溶质的成分是什么?
【猜想假设】
猜想一:NaOH
猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3
猜想四:Ca(OH)2、Na2CO3
其中猜想四不合理,请用化学方程式说明原因Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【实验探究】
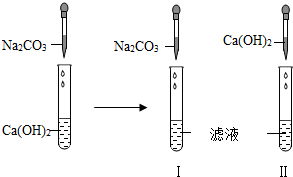
【实验反思】小文认为该实验方案并未证明猜想一是否成立,应补充相关实验予以证明,你是否赞同?否(填“是”或“否”),针对猜想三,还可以设计新方案:取少量滤液于试管中,滴入足量稀盐酸,实验现象为产生气泡.
【实验结论】猜想三正确.
【提出问题】滤液中溶质的成分是什么?
【猜想假设】
猜想一:NaOH
猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3
猜想四:Ca(OH)2、Na2CO3
其中猜想四不合理,请用化学方程式说明原因Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【实验探究】

| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液于试管Ⅰ中,向其中滴入适量Na2CO3溶液 | 无白色沉淀产生 | 猜想二不成立 |
| 取少量滤液于试管Ⅱ中,向其中滴入适量Ca(OH)2溶液 | 产生白色沉淀 | 猜想三成立 |
【实验结论】猜想三正确.
19.下列实验现象描述正确的是( )
| A. | 电解水时,正、负电极上产生气体的体积比为2:1 | |
| B. | 木炭在空气中完全燃烧后生成黑色固体 | |
| C. | 铁在氧气中燃烧生成物为熔融状 | |
| D. | 打开一片浓盐酸,瓶口会出现白色烟雾 |
13.以下常州市各文化遗产的生产工艺,主要涉及化学变化的是( )
| A. | 木梳制作 | B. | 黄酒酿造 | C. | 乱针绣 | D. | 竹刻工艺 |
 燃气灶能效标准将于2015年4月1日正式实施,这标志着与市民生活息息相关的燃气灶将进入节能时代,如图是一款燃气灶的示意图:
燃气灶能效标准将于2015年4月1日正式实施,这标志着与市民生活息息相关的燃气灶将进入节能时代,如图是一款燃气灶的示意图: