题目内容
7.等质量、等溶质质量分数的氢氧化钠溶液和硫酸充分反应后,所得溶液中的离子有Na+、SO42-?、OH-?,有关反应的化学方程式为2NaOH+H2SO4═Na2SO4+2H2O.分析 根据化学方程式的有关计算,可知等质量的氢氧化钠和硫酸反应,氢氧化钠有剩余.
解答 解:2NaOH+H2SO4=Na2SO4+2H2O
80 98
由以上关系可知,等质量的氢氧化钠和硫酸反应,氢氧化钠有剩余,故反应完毕后,溶液中的溶质有硫酸钠和氢氧化钠两种,故溶液中的离子有Na+、
SO42-?、OH- 反应的化学方程式为2NaOH+H2SO4═Na2SO4+2H2O
故答案为:Na+、SO42-?、OH-??2NaOH+H2SO4═Na2SO4+2H2O
点评 本题考查了中和反应的应用,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
17.下列实验现象描述错误的是( )
| A. | 二氧化硫通入稀高锰酸钾溶液中,溶液褪色 | |
| B. | 浓硝酸滴入蛋清溶液中,微热,出现黄色沉淀 | |
| C. | 铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 二氧化碳通入氯化钙溶液中,产生白色沉淀 |
2.测定白醋的 pH 时,先用蒸馏水润湿 pH 试纸,则所测得白醋的 pH 将( )
| A. | 偏小 | B. | 偏大 | C. | 不变 | D. | 无法判断 |
12.如图是某化学反应的微观示意图.下列说法错误的是( )


| A. | 该反应前后元素种类不变 | |
| B. | 反应前后氯元素共显示三种化合价 | |
| C. | 参加反应的两物质的质量比为 1:1 | |
| D. | 反应后的物质溶于水形成的溶液的 pH<7 |
17.下列气体既可以用氢氧化钠干燥,又可以用浓硫酸干燥的是( )
| A. | HCl | B. | O2 | C. | NH3 | D. | SO2 |
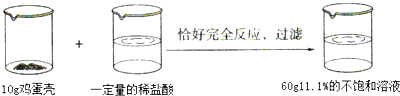
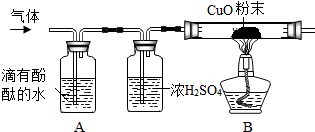
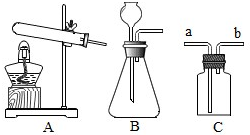 根据装置图回答下列问题:
根据装置图回答下列问题: