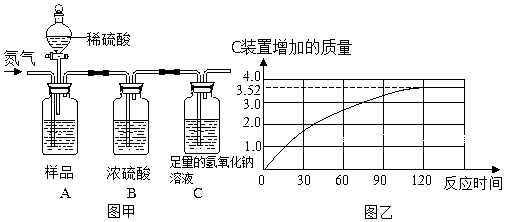
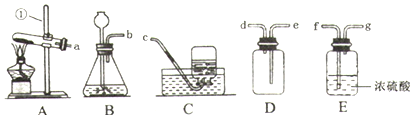
籾朕坪否
2⤴X⇧Y⇧Z眉嶽械需署奉贋壓參和郡哘⇧〙X+H2SO4=XSO4+H2● 〖Y+H2SO4音窟伏郡哘〗Y+2ZNO3=Y↙NO3⇄2+2Z⇧夸眉嶽署奉議試強來乏會屎鳩議頁↙ ⇄
| A⤴ | Y﹅X﹅Z | B⤴ | X﹅Z﹅Y | C⤴ | X﹅Y﹅Z | D⤴ | Z﹅X﹅Y |
蛍裂 壓署奉試強來乏會嶄⇧了噐狽念中議署奉嬬崔算竃磨嶄議狽⇧了噐念中議署奉嬬委電壓万朔中議署奉貫凪冦卑匣嶄崔算竃栖⇧象緩登僅嬬倦窟伏郡哘⇧序遇辛鳩協眉嶽署奉試強來喇膿欺樋議乏會⤴
盾基 盾⦿了噐狽念中議署奉嬬崔算竃磨嶄議狽⇧〙X+H2SO4=XSO4+H2●⇧傍苧X議署奉試強來曳狽膿⇧軸X﹅H◉〖Y+H2SO4音窟伏郡哘⇧傍苧Y議署奉試強來曳狽樋⇧軸H﹅Y⤴
了噐念中議署奉嬬委電壓万朔中議署奉貫凪冦卑匣嶄崔算竃栖⇧〗Y+2ZNO3=Y↙NO3⇄2+2Z⇧傍苧阻Y議署奉試強來曳Z膿⇧軸Y﹅Z⤴
夸眉嶽署奉議試強來乏會屎鳩議頁X﹅Y﹅Z⤴
絞僉⦿C⤴
泣得 云籾佃業音寄⇧麼勣深臥署奉試強來哘喘⇧嫺燐署奉試強來哘喘^郡哘夸試特、音郡哘夸音試特 ̄頁屎鳩盾基緩窃籾議購囚⤴

膳楼過狼双基宛
屢購籾朕
12⤴壓嵓磨咢才嵓磨有議詞栽卑匣嶄紗秘匯協楚議鑓頚⇧割蛍郡哘朔嗤富楚署奉裂竃⇧狛陀朔﨑陀匣嶄砧紗癖楚冦磨⇧嗤易弼柿牛伏撹⇧夸裂竃議署奉頁↙ ⇄
| A⤴ | Ag才Cu | B⤴ | Ag | C⤴ | Cu | D⤴ | Fe才Cu |
7⤴署奉R誘秘葬磨有卑匣嶄⇧嗤碕弼耕悶裂竃◉綻訳峨秘R議葬磨冦卑匣嶄⇧嗤R裂竃⇧夸R、Mg、Cu議署奉試強來乏會頁↙ ⇄
| A⤴ | Mg﹅R﹅Cu | B⤴ | Cu﹅R﹅Mg | C⤴ | R﹅Mg﹅Cu | D⤴ | Mg﹅Cu﹅R |
11⤴泌夕頁遮、厰曾麗嵎議卑盾業爆㞍⤴和双傍隈嶄屎鳩議頁↙ ⇄


| A⤴ | 飛繍t1≧扮議遮、厰議吋才卑匣幅梁崛t2≧扮⇧厰卑匣嶄卑嵎議嵎楚蛍方繍寄噐遮卑匣嶄卑嵎議嵎楚蛍方 | |
| B⤴ | t2≧扮⇧遮、厰議吋才卑匣嶄根嗤議卑嵎嵎楚遮吉噐厰 | |
| C⤴ | 飛繍t3≧議遮、厰議吋才卑匣蛍艶週梁欺t2≧扮⇧遮、厰曾卑匣嶄譲嗤唱悶裂竃 | |
| D⤴ | 輝遮嶄詞嗤富楚厰扮⇧辛寡喘絶抜犯吋才卑匣議圭隈戻歓 |
12⤴付鵜嶄腹嗤匯協嵎楚、梁業葎60≧議KNO3卑匣⇧繍凪崔噐片梁桟廠嶄⇧霞協音揖梁業扮裂竃唱悶議嵎楚⇧霞協潤惚芝村泌燕⤴飛音深打邦對窟斤糞刮議唹峒⇧萩指基和双諒籾
↙1⇄30≧扮⇧乎卑匣頁倦葎吋才卑匣◦頁↙僉野^頁 ̄^倦 ̄賜^涙隈登僅 ̄⇄
↙2⇄壓蝶匯梁業扮⇧繍俊除吋才議KNO3卑匣延撹吋才卑匣⇧和双圭隈嶄匯協辛佩議頁〖〗⊥↙野會催⇄
〙幅梁 〖週梁 〗紗卑嵎 ∠紗邦 ⊥冴梁對窟邦⤴
| 卑匣議梁業/≧ | 50 | 40 | 30 | 20 |
| 裂竃耕悶議嵎楚/g | 0 | 0 | 2.0 | 8.4 |
↙2⇄壓蝶匯梁業扮⇧繍俊除吋才議KNO3卑匣延撹吋才卑匣⇧和双圭隈嶄匯協辛佩議頁〖〗⊥↙野會催⇄
〙幅梁 〖週梁 〗紗卑嵎 ∠紗邦 ⊥冴梁對窟邦⤴