题目内容
下列物质加入或通入紫色石蕊试液中试液会变色的是( )
| A、二氧化碳 | B、活性炭 |
| C、氯化钠 | D、氯化镁 |
考点:酸碱指示剂及其性质
专题:常见的酸 酸的通性
分析:石蕊溶液遇酸性溶液变红色,遇碱性溶液变蓝色,据此结合二氧化碳的化学性质、活性炭具有吸附性、常见溶液的酸碱性,进行分析判断即可.
解答:解:A、二氧化碳能与水反应生成碳酸,通入紫色石蕊试液中试液会变红色,故选项正确.
B、活性炭具有吸附性,能吸附异味和色素,加入紫色石蕊试液中试液会变无色,故选项正确.
C、氯化钠的水溶液显中性,加入紫色石蕊试液中试液会不变色,故选项错误.
D、氯化镁的水溶液显中性,加入紫色石蕊试液中试液会不变色,故选项错误.
故选:AB.
B、活性炭具有吸附性,能吸附异味和色素,加入紫色石蕊试液中试液会变无色,故选项正确.
C、氯化钠的水溶液显中性,加入紫色石蕊试液中试液会不变色,故选项错误.
D、氯化镁的水溶液显中性,加入紫色石蕊试液中试液会不变色,故选项错误.
故选:AB.
点评:本题难度不大,掌握石蕊溶液的性质、二氧化碳的化学性质、活性炭具有吸附性、常见溶液的酸碱性是正确解答本题的关键.

练习册系列答案
相关题目
下列物质间的转化,不能一步实现的是( )
| A、Fe→FeCl3 |
| B、CO2→CaCO3 |
| C、Cu0→CuCl2 |
| D、MgCl2→KCl |
下列各组物质按照单质、氧化物、混合物的顺序排列的是( )
| A、氮气 氧气 空气 |
| B、石墨 熟石灰 生石灰 |
| C、水银 水 糖水 |
| D、冰 干冰 醋酸 |
在氢氧化钠溶液中加入一定量的稀硫酸后,下列实验能证明两者恰好完全中和的是( )
| A、滴入适量FeCl3溶液,溶液变黄,但无沉淀生成 |
| B、滴入几滴酚酞试液,酚酞试液不变色 |
| C、滴入适量BaCl2溶液和稀硝酸,观察到有白色沉淀 |
| D、测得反应后溶液中Na+与SO42-个数比为2:1 |
造成温室效应的物质是( )
| A、臭氧和一氧化碳 |
| B、二氧化硫和二氧化氮 |
| C、甲烷和二氧化碳 |
| D、二氧化碳和一氧化碳 |
 如图所示,大试管底部有螺旋状的光亮的铁丝,把试管倒插入水中,放置一周后,观察到铁丝表面有
如图所示,大试管底部有螺旋状的光亮的铁丝,把试管倒插入水中,放置一周后,观察到铁丝表面有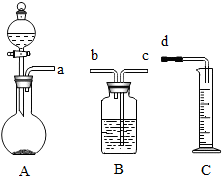 某兴趣小组用如图所示装置收集并测量反应产生的气体及其体积.若用该装置制取氢气,通过分液漏斗中加入30mL稀盐酸,与平底烧瓶中盛放的0.65g锌粒充分反应(盐酸足量).回答下列问题:
某兴趣小组用如图所示装置收集并测量反应产生的气体及其体积.若用该装置制取氢气,通过分液漏斗中加入30mL稀盐酸,与平底烧瓶中盛放的0.65g锌粒充分反应(盐酸足量).回答下列问题: