题目内容
某课外活动小组进行如下实验探究。
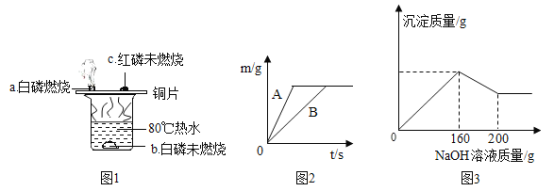
(1)验证物质的燃烧条件
根据图1进行实验,实验现象如图所示.80℃热水的作用是_____。
(2)①将一定质量的锌粒投入含有 Cu(NO3)2 和 Fe(NO3)2 的混合溶液中,充分反应后过滤,若滤液中只含一种溶质,则滤渣中一定含有_____。(填化学用语)
②在质量相等、溶质质量分数相同的稀硫酸中,分别加入等质量的锌粉和铁粉,生成氢气质量(m)随反应时间(t)的变化曲线如图 2 所示。下列表述不正确的是_____(填序号)。
a表示锌和稀硫酸的反应曲线 b反应结束后消耗两种金属的质量相等
c反应结束后两种金属一定都有剩余 d反应结束后稀硫酸都没有剩余
e反应结束后生成的氢气质量相等。
(3)已知氢氧化铝能溶解在过量的氢氧化钠溶液中生成偏铝酸钠(NaAlO2)溶液,有关化学方程式为:Al(OH)3+NaOH=NaAlO2+2H2O.现有某无色溶液,可能含有盐酸、硫酸镁、硝酸钾、硫酸铜、氯化铝、碳酸钠中的一种或数种。取一定量该溶液于烧杯中,往其中逐滴加入 NaOH 溶液,产生沉淀的质量与加入NaOH溶液的质量关系如图3所示。推断在该溶液中一定存在的物质是_____,一定不存在的物质是_____,可能存在的物质是_____。
 学习实践园地系列答案
学习实践园地系列答案以孔雀石为原料制取胆矾(CuSO4?5H2O)的部分工艺流程如图所示。

(查阅资料)
I.孔雀石主要成分为Cu2(OH)2CO3,还有少量SiO2(难溶于水、不与稀硫酸反应)、Fe2O3等杂质。
Ⅱ.胆矶是一种蓝色晶体,受热易分解。
Ⅲ.在该实验条件下,Fe(OH)3、Cu(OHI)2沉淀的pH如下表:
Fe(OH)3 | Cu(OH)2 | |
开始沉淀的pH | 1.14 | 4.2 |
完全沉淀的pH | 3.0 | 6.7 |
(1)操作1的名称为_____,实验室进行该操作时玻璃棒的作用是_____。
(2)气体a生成CaCO3的同时还生成NH4C1,该反应的化学方程式为_____。
(3)溶液c中的溶质有:CuSO4、H2SO4和_____(写化学式)
(4)为将溶液中的Fe3+全部转化为Fe(OH)3,沉淀而Cu2+不转化为Cu(OH)2沉淀,应调节pH=m,m的范围是_____。
(5)获得胆矾晶体时采用降温结晶而不用蒸发结晶的主要原因是_____。
研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:

(假设)H2O2生成O2的快慢与催化剂种类有关
(实验方案)常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量MnO2和红砖粉,测量各生成一瓶(相同体积)O2所需要的时间。
(进行实验)如图是他们进行实验的装置图,此实验中B处宜采用的气体收集方法是_____。
(实验记录)
实验编号 | 1 | 2 |
反应物 | 6% H2O2 | 6% H2O2 |
催化剂 | 1g 红砖粉 | 1g MnO2 |
时间 | 152s | 35s |
(结论)该探究过程得出的结论是_____。
(反思)H2O2在常温下分解缓慢,加入MnO2或 红砖粉后反应明显加快,若要证明MnO2和红砖粉是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的_____和_____是否改变。
H2O2生成O2的快慢还与哪些因素有关?请你帮助他们继续探究。(只要求提出一种假设和实验方案)
(假设)_____。
(实验方案)_____。



 给液体加热 B.
给液体加热 B.  取用液体药品
取用液体药品 熄灭酒精灯 D.
熄灭酒精灯 D. 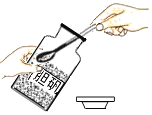 取用固体药品
取用固体药品 向一定量的稀硫酸中逐滴加入氢氧化钡溶液至恰好完全反应
向一定量的稀硫酸中逐滴加入氢氧化钡溶液至恰好完全反应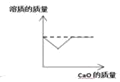 向一定量的水中加入生石灰
向一定量的水中加入生石灰 向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液
向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液 往硫酸钠和盐酸的混合溶液中加入氢氧化钡溶液
往硫酸钠和盐酸的混合溶液中加入氢氧化钡溶液