题目内容
12.锌、铁与相同浓度的稀硫酸反应生成相同质量的氢气,下列说法中不正确的是( )| A. | 参与反应酸的量可能不足 | |
| B. | 消耗锌的质量比消耗铁的质量少 | |
| C. | 消耗稀硫酸中溶质的质量相等 | |
| D. | 相同条件下,锌与稀硫酸反应比铁与稀硫酸反应快 |
分析 锌和稀硫酸反应生成硫酸锌和氢气,铁和稀硫酸反应生成硫酸亚铁和氢气,生成的氢气中的氢元素完全来自于硫酸.
解答 解:A、因为生成的氢气中的氢元素完全来自于硫酸,如果参与反应酸的量不足,锌和铁过量时生成的氢气质量相等,该选项说法正确;
B、锌、铁和稀硫酸反应的化学方程式及其质量关系为:
Zn+H2SO4═ZnSO4+H2↑,Fe+H2SO4═FeSO4+H2↑,
65 2 56 2
由以上质量关系可知,生成氢气质量相等时,消耗锌的质量比消耗铁的质量大,该选项说法不正确;
C、因为生成的氢气中的氢元素完全来自于硫酸,则锌、铁与相同浓度的稀硫酸反应生成相同质量的氢气时,消耗稀硫酸中溶质的质量相等,该选项说法正确;
D、锌比铁活泼,因此相同条件下,锌与稀硫酸反应比铁与稀硫酸反应快,该选项说法正确.
故选:B.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.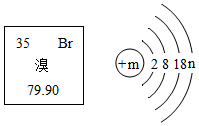 溴元素在元素周期表中的信息与溴原子结构示意图如图所示,下列说法正确的是( )
溴元素在元素周期表中的信息与溴原子结构示意图如图所示,下列说法正确的是( )
 溴元素在元素周期表中的信息与溴原子结构示意图如图所示,下列说法正确的是( )
溴元素在元素周期表中的信息与溴原子结构示意图如图所示,下列说法正确的是( )| A. | 溴相对原子质量为79.90g | |
| B. | 溴原子质量由构成其原子的质子和电子决定 | |
| C. | 溴元素属于金属元素 | |
| D. | m=35、n=7 |
20.我国科学家已研制出新型高效光催化剂作用下,利用太阳能分解水制取氢气.水在通过并接触催化剂表面时,分解的微观过程用示意图表示如下:(“○”表示氢原子,“●”表示氧原子,“ ”表示催化剂).则水分解微观过程的正确顺序是 ( )
”表示催化剂).则水分解微观过程的正确顺序是 ( )

 ”表示催化剂).则水分解微观过程的正确顺序是 ( )
”表示催化剂).则水分解微观过程的正确顺序是 ( )
| A. | ①②③④⑤ | B. | ③⑤②④① | C. | ①④②⑤③ | D. | ①④⑤②③ |
7.空气中含量较多,且能用于填充食品包装袋的气体是( )
| A. | 氮气 | B. | 氧气 | C. | 稀有气体 | D. | 氢气 |
4.对某无色溶液所含溶质的分析,合理的是( )
| A. | NaOH、Na2CO3、NaCl | B. | KNO3、NaCl、FeCl2 | ||
| C. | HCl、NaOH、NaCl | D. | Na2CO3、Ca(OH)2、NaCl |
