题目内容
硫酸钠是制造纸浆、染料稀释剂、医药品等的重要原料。某硫酸钠粗品中含有少量CaCl2和MgCl2,实验室进行提纯的流程如下:
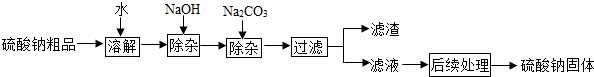
回答下列问题:
(1)用Na2CO3除杂的化学方程式为: 。
(2)NaOH和Na2CO3如果添加过量了,可加入适量_________溶液除去。请任写出一个相关反应的化学方程式: 。
(3)“后续处理”的主要操作是蒸发,为了获得纯净的硫酸钠,应蒸发至 。
A.完全蒸干时停止加热 (填序号)
B.快干时停止加热,利用余热蒸干
C.有大量固体析出时停止加热,过滤弃去剩余的少量溶液
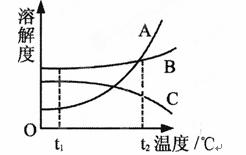
(4)已知硫酸 钠的溶解度随温度变化的曲线如图所示。
钠的溶解度随温度变化的曲线如图所示。
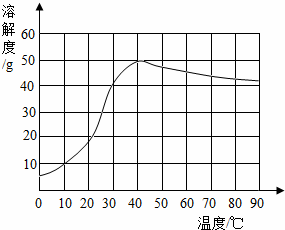
40℃时,100g蒸馏水中溶解 g硫酸钠达到饱和。将该饱和溶液升高温度至90℃,观察到的现象是 。
(1)Na2CO3+CaCl2==2NaCl+CaCO3↓
(2) 稀硫酸
Na2CO3+H2SO4= Na2SO4+H2O+CO2↑或2NaOH+H2SO4=Na2SO4+2H2O
Na2SO4+H2O+CO2↑或2NaOH+H2SO4=Na2SO4+2H2O
(3)C (4) 50 有固体析出

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
 甲、乙两种固体物质的溶解度曲线。下列说法错误的是 ( )
甲、乙两种固体物质的溶解度曲线。下列说法错误的是 ( )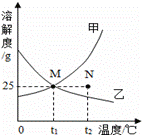
 酿酒 D、原子弹爆炸
酿酒 D、原子弹爆炸