题目内容
8.在一密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:| 物质 | A | B | C | D |
| 反应前质量(g) | 4 | 6 | 111 | 4 |
| 反应后质量(g) | m | 15 | 0 | 84 |
(2)密闭容器中发生的化学变化属于分解反应;
(3)该反应中各物质的质量比为22:9:111:80.
分析 反应后B质量增加9g,是生成物;
反应后C质量减少111g,是反应物;
反应后D质量增加80g,是生成物;
根据质量守恒定律可知,A是生成物,生成的质量为:111g-9g-80g=22g.
解答 解:(1)反应后A的质量为:22g+4g=26g.
故填:26;
(2)该反应中,反应物是一种,生成物是三种,属于分解反应.
故填:分解.
(3)反应中参加反应的A、B、C、D质量比为:22g:9g:111g:80g=22:9:111:80.
故填:22:9:111:80.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、进行相关方面计算的基础

练习册系列答案
相关题目
18.H2、C、CO均可与氧化铜粉末发生反应,对三个反应的说法中不正确的是( )
| A. | 都属于置换反应 | B. | 三种物质均发生了氧化反应 | ||
| C. | 都有红色的铜生成 | D. | 反应中氧化铜均被还原 |

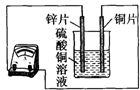 如图所示,该同学用导线将锌片和铜片连接起来,接入电流表,然后把它们一起插入硫酸铜溶液中,该实验的现象为:①电流表指针发生偏转;②铜片表面附着一层红色固体.
如图所示,该同学用导线将锌片和铜片连接起来,接入电流表,然后把它们一起插入硫酸铜溶液中,该实验的现象为:①电流表指针发生偏转;②铜片表面附着一层红色固体.