题目内容
20.对比学习有利于发现事物的共性与个性,为探究酸的性质,同学们进行了如下实验:| 实验内容 | 实验现象 | 分析与结论 |
 | 两试管中均产生气泡 | (1)不同的酸具有相似的性质,这是因为酸的溶液中都含有氢离子 |
 | C试管中产生白色沉淀, D试管中无明显现象 | (2)不同的酸根会导致酸的“个性”差异.因此,可用氯化钡溶液鉴别盐酸和硫酸 |
分析 (1)根据酸的溶液中含有的共同的离子分析;
(2)根据稀硫酸与氯化钡的反应分析;
(3)根据反应的现象和反应物的量分析发生的反应.
解答 解:(1)由上述实验可知,稀硫酸、稀盐酸都能与碳酸钠反应生成了气体,不同的酸具有相似的性质,这是因为酸的溶液中都含有氢离子;
(2)由于稀硫酸与氯化钡反应生成了硫酸钡沉淀和盐酸,所以,C试管中产生白色沉淀;
(3)由题意可知,将A、D两试管中的无色液体同时倒入一个洁净的废液缸,废液缸中立刻冒气泡并出现白色沉淀,说明了碳酸钠有剩余,与盐酸发生了反应,化学方程式为:2HCl+Na2CO3═2NaCl+H2O+CO2↑,由于硫酸钠与氯化钡反应生成了硫酸钡沉淀,若盐酸的量不足,剩余的碳酸钠能与氯化钡反应生成了碳酸钡沉淀,所以,最终产生白色沉淀中一定有硫酸钡,可能有BaCO3.
故答为:(1)氢离子;(2)白色沉淀;(3)2HCl+Na2CO3═2NaCl+H2O+CO2↑,BaCO3.
点评 这类题目主要是结合问题情景,通过分析、提炼常见酸碱的物理特性和化学性质,来补全实验设计中的空白,或者科学地设计实验方案,或者进行简单计算等等.要想解答好这类题目,就必须根据所学认真、规范地填写好每一个小题.特别是猜想、操作、现象的描述要准确、精炼,绝不可出现错别字;化学方程式的书写和计算都要严格按照步骤正确的进行书写和计算,切不可丢三落四.

练习册系列答案
相关题目
4.下列物质的用途与性质不对应的是( )
| 物质 | 用途 | 性质 | |
| A | 甲烷 | 作燃料 | 吸收红外辐射的能力很强 |
| B | 熟石灰 | 改良酸性土壤 | 熟石灰能与酸发生中和反应 |
| C | 小苏打 | 治疗胃酸过多 | 小苏打能与盐酸反应 |
| D | 钛 | 制作医疗器械 | 对人体无毒性,不与肌肉骨骼反应 |
| A. | A | B. | B | C. | C | D. | D |
8. 甲同学认为Ca(OH)2与CO2反应,而NaOH与CO2不能反应,因为实验室里检验CO2用Ca(OH)2溶液而不用NaOH溶液.乙同学认为甲同学的说法不完全正确.请你帮助乙同学完成以下实验来证明他的观点.
甲同学认为Ca(OH)2与CO2反应,而NaOH与CO2不能反应,因为实验室里检验CO2用Ca(OH)2溶液而不用NaOH溶液.乙同学认为甲同学的说法不完全正确.请你帮助乙同学完成以下实验来证明他的观点.
(1)[提出假设]:NaOH与CO2能反应
(2)[设计方案]:①用石灰石和稀盐酸制取CO2气体;
②用如图装置(软塑料瓶和盖)与发生装置组装来收集干燥的CO2气体的做法是软塑料瓶瓶口向上,将导气管伸入到塑料瓶的底部
③验证假设
所以假设成立.
(4)[总结与反思]实验室里NaOH溶液易变质,其化学方程式为:2NaOH+CO2=Na2CO3+H2O;所以NaOH溶液应密封保存.
 甲同学认为Ca(OH)2与CO2反应,而NaOH与CO2不能反应,因为实验室里检验CO2用Ca(OH)2溶液而不用NaOH溶液.乙同学认为甲同学的说法不完全正确.请你帮助乙同学完成以下实验来证明他的观点.
甲同学认为Ca(OH)2与CO2反应,而NaOH与CO2不能反应,因为实验室里检验CO2用Ca(OH)2溶液而不用NaOH溶液.乙同学认为甲同学的说法不完全正确.请你帮助乙同学完成以下实验来证明他的观点.(1)[提出假设]:NaOH与CO2能反应
(2)[设计方案]:①用石灰石和稀盐酸制取CO2气体;
②用如图装置(软塑料瓶和盖)与发生装置组装来收集干燥的CO2气体的做法是软塑料瓶瓶口向上,将导气管伸入到塑料瓶的底部
③验证假设
| 实验步骤 | 实验现象 | 结论 |
| 第一步:向集满CO2软塑料瓶中注入少量的NaOH溶液立即选好盖子,振荡 | 瓶子变瘪了 | NaOH溶液吸收了塑料瓶中的CO2气体. |
| 第二步:取上一步中所得溶液,加入盐酸 | 有大量气泡生成 | 化学方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
(4)[总结与反思]实验室里NaOH溶液易变质,其化学方程式为:2NaOH+CO2=Na2CO3+H2O;所以NaOH溶液应密封保存.
5.在做锌与稀硫酸反应实验时,兴趣小组的同学发现试管中产生气泡的速度先变快后变慢.这一现象引起了同学们的思考,化学反应的快慢会受到哪些因素的影响?他们设计了如下的实验方案进行探究:分三次取足量的相同质量的稀硫酸,分别与大小、性状、质量相同的锌粒进行反应.实验数据记录如表.
(1)化学反应过程中常伴随着能量变化,由实验可知,锌与稀硫酸反应时会放出(填“放出”或“吸收”)热量.
(2)根据实验数据可以得出锌与稀硫酸反应的快慢与温度、反应物的浓度有关.
(3)同学们发现3次实验过程中,产生的气泡在开始阶段逐渐变快,一定时间后逐渐变慢至停止.根据实验数据分析,锌与稀硫酸反应一定时间后产生气泡逐渐变慢的原因是开始反应,随着反应进行溶液的温度升高,反应加快,后来温度升高变慢,溶液中溶质的质量分数变小,反应变慢.
| 实验编号 | 1 | 2 | 3 | |
| 稀硫酸的溶质质量分数 | 10% | 10% | 20% | |
| 溶液温度/℃ | 反应前 | 20 | 30 | 20 |
| 完全反应后 | 26 | 27 | 28 | |
| 完全反应所需时间 | 长 | 较短 | 较短 | |
(2)根据实验数据可以得出锌与稀硫酸反应的快慢与温度、反应物的浓度有关.
(3)同学们发现3次实验过程中,产生的气泡在开始阶段逐渐变快,一定时间后逐渐变慢至停止.根据实验数据分析,锌与稀硫酸反应一定时间后产生气泡逐渐变慢的原因是开始反应,随着反应进行溶液的温度升高,反应加快,后来温度升高变慢,溶液中溶质的质量分数变小,反应变慢.
9.如图所示的基本实验操作符合操作规范的是( )
| A. | 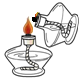 点燃酒精灯 | B. | 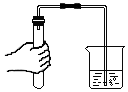 检查气密性 | C. | 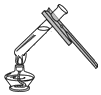 给液体加热 | D. | 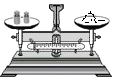 称量药品质量 |
10.如图化学实验操作中,不正确的是( )
| A. | 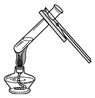 | B. | 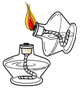 | C. | 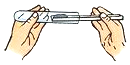 | D. | 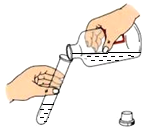 |