题目内容
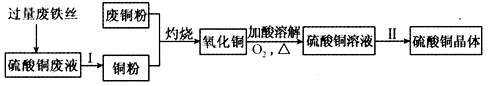
利用废铁丝、硫酸铜废液(含硫酸亚铁)和废铜粉制备硫酸铜晶体.生产过程如下: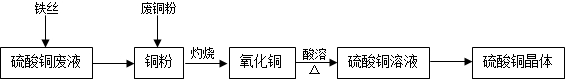
试回答下列问题:
(1)铁丝投入到硫酸铜溶液里发生反应的类型是
(2)从硫酸铜溶液得到硫酸铜晶体过程叫做
(3)为使灼烧后的氧化铜(含有少量铜)混合物充分酸溶,在加入稀硫酸的同时,还通入氧气.通入氧气的目的是
分析:(1)铁能与硫酸铜发生置换反应,生成硫酸亚铁和铜,根据反应的特点判断反应的类型;铁丝保存时会在空气中生锈,可使用稀硫酸除去表面的铁锈,以便与硫酸铜发生反应;
(2)从溶液中析出晶体的过程称为结晶;
(3)为使灼烧过程中没完全反应的铜能与稀硫酸反应充分反应,通入氧气把少量的铜氧化成能与稀硫酸发生反应的氧化铜.
(2)从溶液中析出晶体的过程称为结晶;
(3)为使灼烧过程中没完全反应的铜能与稀硫酸反应充分反应,通入氧气把少量的铜氧化成能与稀硫酸发生反应的氧化铜.
解答:解:(1)投入的铁丝与硫酸铜发生反应生成铜和硫酸亚铁,反应为一种单质与一种化合物生成一种单质和一种化合物的置换反应;利用硫酸能与金属氧化物反应,把铁丝用稀硫酸处理除去表面的氧化物;
(2)硫酸铜溶液中析出硫酸铜晶体的过程称为结晶;
(3)通入的氧气继续与少量的铜反应生成能与稀硫酸反应的氧化铜,使铜全部转化为硫酸铜;反应的化学方程式为2Cu+O2?2CuO,CuO+H2SO4═CuSO4+H2O;
故答案为:
(1)置换反应;除去铁丝表层的氧化物;
(2)结晶;
(3)2Cu+O2
2CuO,CuO+H2SO4═CuSO4+H2O(或2Cu+O2+2H2SO4
2CuSO4+2H2O).
(2)硫酸铜溶液中析出硫酸铜晶体的过程称为结晶;
(3)通入的氧气继续与少量的铜反应生成能与稀硫酸反应的氧化铜,使铜全部转化为硫酸铜;反应的化学方程式为2Cu+O2?2CuO,CuO+H2SO4═CuSO4+H2O;
故答案为:
(1)置换反应;除去铁丝表层的氧化物;
(2)结晶;
(3)2Cu+O2
| ||
| ||
点评:根据金属的活动性顺序表,位于氢之前的金属能与酸发生置换反应,而位于氢之后的金属不能与酸发生反应;活动性强的金属能将活动性弱的金属从其盐溶液中置换出来.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目


 金属材料在生产、生活中应用广泛.
金属材料在生产、生活中应用广泛.

 2CuO
2CuO 2CuSO4+2H2O
2CuSO4+2H2O

 2CuO
2CuO 2CuSO4+2H2O
2CuSO4+2H2O

 2CuO
2CuO 2CuSO4+2H2O
2CuSO4+2H2O