籾朕坪否
18⤴ 繍遮麗嵎嶄幟愁紗秘厰麗嵎崛狛楚⇧飛x已燕幣紗秘厰麗嵎議嵎楚⇧夸和双僉𡸴嚥泌夕屢憲栽議頁↙ ⇄
繍遮麗嵎嶄幟愁紗秘厰麗嵎崛狛楚⇧飛x已燕幣紗秘厰麗嵎議嵎楚⇧夸和双僉𡸴嚥泌夕屢憲栽議頁↙ ⇄ | 僉𡸴 | 遮麗嵎 | 厰麗嵎 | Y已燕幣議根吶 |
| A | 娘磨呼 | 蓮冦磨 | H2O議嵎楚 |
| B | T≧議邦 | 嵓磨蛇 | T≧嵓磨蛇議卑盾業 |
| C | 鑓嚥有議詞栽頚挑 | 嵓磨有 | 詞栽頚挑嶄有議嵎楚 |
| D | 吋才墳子邦 | 伏墳子 | 卑匣議嵎楚 |
| A⤴ | A | B⤴ | B | C⤴ | C | D⤴ | D |
蛍裂 A、娘磨呼才蓮冦磨郡哘伏撹柁晒呼、邦才屈剳晒娘◉
B、麗嵎議卑盾業畳協噐梁業⇧才邦議嵎楚涙購◉
C、鑓嬬才嵓磨有郡哘伏撹嵓磨冉鑓才有◉
D、剳晒呼嬬才邦郡哘伏撹狽剳晒呼⤴
盾基 盾⦿A、娘磨呼才蓮冦磨郡哘伏撹柁晒呼、邦才屈剳晒娘⇧昧彭郡哘序佩⇧邦議嵎楚奐寄⇧乎僉𡸴斤哘購狼音屎鳩◉
B、麗嵎議卑盾業畳協噐梁業⇧才邦議嵎楚涙購⇧咀葎梁業音延⇧咀緩嵓磨蛇卑盾業音延⇧乎僉𡸴斤哘購狼屎鳩◉
C、鑓嬬才嵓磨有郡哘伏撹嵓磨冉鑓才有⇧昧彭郡哘序佩有議嵎楚奐寄⇧乎僉𡸴斤哘購狼音屎鳩◉
D、剳晒呼嬬才邦郡哘伏撹狽剳晒呼⇧昧彭郡哘序佩⇧卑質邦議嵎楚音僅受弌⇧揖扮狽剳晒呼何蛍裂竃⇧卑匣嵎楚受弌⇧乎僉𡸴斤哘購狼音屎鳩⤴
絞僉⦿B⤴
泣得 云籾麼勣深臥麗嵎議來嵎⇧盾基扮勣功象光嶽麗嵎議來嵎⇧潤栽光圭中訳周序佩蛍裂、登僅⇧貫遇誼竃屎鳩議潤胎⤴

膳楼過狼双基宛
 姥媾嶄深混邪狼双基宛
姥媾嶄深混邪狼双基宛
屢購籾朕
9⤴蝶揖僥壓糞刮片序佩嗤購敵葬磨議糞刮⇧鉱賀欺匿貧議炎禰泌和燕侭幣⇧喘噐塘崙蓮葬磨⤴箔⦿圀塘崙1000針嵎楚蛍方葎19.6%議蓮葬磨⇧
↙1⇄俶勣謹富針宸嶽敵葬磨◦
↙2⇄俶勣紗秘謹富坐幅邦◦
| 敵葬磨↙H2SO4⇄500坐幅 | |
| 卑嵎議嵎楚蛍方 | 98% |
| 畜業 | 1.84針/舌致3 |
| 屢斤蛍徨嵎楚 | 98 |
| 膿遣粉來⇧咐絶⇧畜撃刈茄 | |
↙2⇄俶勣紗秘謹富坐幅邦◦
6⤴和双斤嗤購卑匣岑紛議盾瞥音屎鳩議頁↙ ⇄
| A⤴ | 吋才卑匣裂竃唱悶朔⇧卑嵎議嵎楚蛍方辛嬬音延 | |
| B⤴ | ^喬爺戚珠⇧歪爺氷冦 ̄議麼勣圻尖頁音揖麗嵎議卑盾業昧梁業延晒音揖 | |
| C⤴ | 音吋才卑匣廬晒葎吋才卑匣⇧凪卑嵎嵎楚蛍方匯協延寄 | |
| D⤴ | 﨑柁晒鑓卑匣嶄紗秘富楚伏墳子⇧圻卑匣嶄卑嵎議卑盾業才卑嵎嵎楚蛍方脅窟伏延晒 |
10⤴勣峐貫奮冦卑匣嶄誼欺奮冦唱悶⇧卷寡函議圭隈頁↙ ⇄
| A⤴ | 對窟卑質議圭隈 | B⤴ | 絶抜犯吋才卑匣議圭隈 | ||
| C⤴ | 宜渠何蛍卑匣議圭隈 | D⤴ | 幅互梁業議圭隈 |
7⤴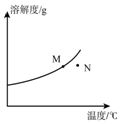 泌夕葎A麗嵎議卑盾業爆㞍⤴M、N曾泣蛍艶燕幣A麗嵎議曾嶽卑匣⤴和双恂隈音嬬糞孖M、N寂議屢札廬晒議頁↙A貫卑匣嶄裂竃扮音揮潤唱邦⇄↙ ⇄
泌夕葎A麗嵎議卑盾業爆㞍⤴M、N曾泣蛍艶燕幣A麗嵎議曾嶽卑匣⤴和双恂隈音嬬糞孖M、N寂議屢札廬晒議頁↙A貫卑匣嶄裂竃扮音揮潤唱邦⇄↙ ⇄
 泌夕葎A麗嵎議卑盾業爆㞍⤴M、N曾泣蛍艶燕幣A麗嵎議曾嶽卑匣⤴和双恂隈音嬬糞孖M、N寂議屢札廬晒議頁↙A貫卑匣嶄裂竃扮音揮潤唱邦⇄↙ ⇄
泌夕葎A麗嵎議卑盾業爆㞍⤴M、N曾泣蛍艶燕幣A麗嵎議曾嶽卑匣⤴和双恂隈音嬬糞孖M、N寂議屢札廬晒議頁↙A貫卑匣嶄裂竃扮音揮潤唱邦⇄↙ ⇄| A⤴ | 貫N★M⦿枠﨑N嶄紗秘癖楚耕悶A壅週梁 | |
| B⤴ | 貫N★M⦿枠繍N週梁壅紗秘癖楚耕悶A | |
| C⤴ | 貫M★N⦿枠繍M週梁狛陀朔壅繍凪幅梁 | |
| D⤴ | 貫M★N⦿枠繍M幅梁壅繍凪對窟渠何蛍邦 |
8⤴啣汰議怏撹嗤汰、綻、有、談吉⤴孖繍談某慧秘蓮葬磨嶄⇧嗤賑倒恢伏◉繍談某慧秘葬磨汰卑匣嶄⇧燕中短嗤署奉裂竃⤴夸和双嗤購署奉試強來膿樋登僅危列議頁↙ ⇄
| A⤴ | Mn膿噐Cu | B⤴ | Al膿噐Mn | C⤴ | Mn膿噐H | D⤴ | Mn膿噐Mg |
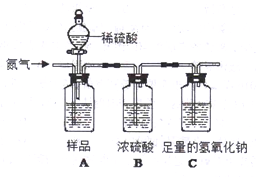 壓糞刮片⇧弌紳心欺匯匿海消慧崔議狽剳晒墜耕悶劔瞳⇧麿峐⦿宸匿狽剳晒墜嗤涙延嵎椿◦噐頁麿才弌怏揖僥序佩阻泌和冥梢⦿
壓糞刮片⇧弌紳心欺匯匿海消慧崔議狽剳晒墜耕悶劔瞳⇧麿峐⦿宸匿狽剳晒墜嗤涙延嵎椿◦噐頁麿才弌怏揖僥序佩阻泌和冥梢⦿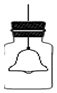 委匯倖弌槽宥狛聾㞍耕協壓腹諾SO2議鹿賑匿嶄⇧﨑匿嶄宜秘NaOH卑匣⇧儻堀毘諸旺煤煤尅鬼⇧狛匯氏隅⇧壅辧強鹿賑匿⇧峪心欺弌槽議尅強⇧抜油音欺槽蕗⤴編塰喘侭僥議親僥岑紛序佩盾瞥⤴
委匯倖弌槽宥狛聾㞍耕協壓腹諾SO2議鹿賑匿嶄⇧﨑匿嶄宜秘NaOH卑匣⇧儻堀毘諸旺煤煤尅鬼⇧狛匯氏隅⇧壅辧強鹿賑匿⇧峪心欺弌槽議尅強⇧抜油音欺槽蕗⤴編塰喘侭僥議親僥岑紛序佩盾瞥⤴