题目内容
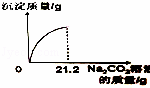
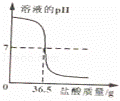
中和反应在工农业生产中应用广泛,现向40g 10%的氢氧化钠溶液中不断滴加盐酸,同时测定溶液pH的变化(曲线如图),请分析计算:
(1)40g 10%的氢氧化钠溶液中含有 4 g的氢氧化钠;当滴入36.5g盐酸时,溶液的pH为 7 .
(2)所用盐酸的溶质质量分数(写出计算过程).
解:
(1)40g 10%的氢氧化钠溶液中含有氢氧化钠的质量为:40g×10%=4g;根据图象可以看出,开始时溶液呈碱性,pH大于7,向氢氧化钠溶液中加入盐酸,盐酸为酸,显酸性,其pH减小,当滴入36.5g盐酸时,溶液的pH为7;
(2)设稀盐酸中溶质的质量为x
NaOH+HCl═NaCl+H2O
40 36.5
4g x
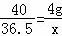
x=3.65g
所用盐酸的溶质质量分数=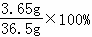 =10%
=10%
答案:所用盐酸的溶质质量分数为10%

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案甲、乙两种物质的溶解度曲线如图所示.下列叙述正确的是( )

|
| A. | 将甲的溶液从t2℃降到t1℃,其溶质的质量分数一定减小 |
|
| B. | t2℃时,甲、乙的饱和溶液各100g,其溶质的质量一定相等 |
|
| C. | 当温度高于0℃而低于t1℃时,乙的溶解度比甲的溶解度大 |
|
| D. | t2℃时,蒸发溶剂可使乙的饱和溶液析出晶体后变为不饱和溶液 |
实验室配制100g 10%的氯化钠溶液,有关实验操作不正确的是( )
|
| A. | 用托盘天平称取10.0g氯化钠 |
|
| B. | 用量筒量取90.0mL 的水 |
|
| C. | 将称取的氯化钠倒入量筒中溶解 |
|
| D. | 将配制的溶液装入试剂瓶中,贴上标签 |
请根据以 下实验装置,回答问题:
下实验装置,回答问题:
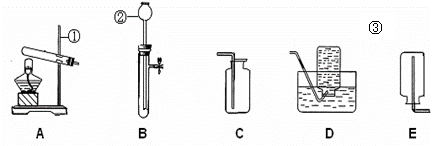 |
(1)写出图中标号仪器的名称:① ________ ②_________③_________
(2)若用A装置制取氧气,实验前要对装置的气密性进行检查:把导管末端浸没在水中,______________________ ,若导管内水柱上升且一段时间不下降,则装置气密性良好;写出实验室用A装置制取氧气的化学方程式 _________________ ,收集氧气可选用D装置,用该装置收集氧气,集满并取出集气瓶后,停止该实验的正确操作步骤是先 ________________后 __________________。
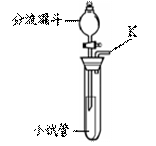
(3)同学们在课外活动中设计了有 关气体的实验。气体的发生
关气体的实验。气体的发生
装置如右图所示。
A、此装置若用于 制备氧气,应在分液漏斗中盛放的药品是
制备氧气,应在分液漏斗中盛放的药品是
___________________;
| 仪器名称 | 分液漏斗 | 小试管 | 大试管 |
| 装置内的药品 | ①________ | ②_________ | 紫色石蕊试液 |
| 大试管中产生的现象及发生反应的化学方程式 | 现象 ③__________________化学方程式④______________ |
B、 此装置还可以验证二氧化碳的化学性质,请完成下表中的内容:
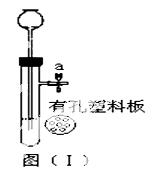
(4) 同学们探究B装置时,对此装置作了改进,改进后的装置如右图(Ⅰ)所示。
改后该装置的优点是 。
(5) 实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控 制加水速度,以免剧烈反应
制加水速度,以免剧烈反应 放热引起发生装置炸裂。你认为B装置应如何改进才符合要求______________________________。
放热引起发生装置炸裂。你认为B装置应如何改进才符合要求______________________________。