题目内容
5. 某无色溶液可能含有氯化钠、氢氧化钠、碳酸钠、硫酸钠、氯化钙中的一种或几种溶质.某化学小组为探究该溶质的成分,进行了如下实验:
某无色溶液可能含有氯化钠、氢氧化钠、碳酸钠、硫酸钠、氯化钙中的一种或几种溶质.某化学小组为探究该溶质的成分,进行了如下实验:Ⅰ.取无色溶液少量,滴加过量氯化钡溶液,过滤,得白色滤渣和无色滤液.
Ⅱ.向步骤Ⅰ所得白色滤渣中加入足量稀硝酸,沉淀全部消失.
Ⅲ.向步骤Ⅰ所得无色滤液中加入足量稀硝酸和硝酸银溶液,产生白色沉淀.
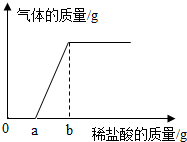
Ⅳ.另取少量原溶液,加入稀盐酸,产生气体的质量与稀盐酸的质量关系如图所示.
请回答下列问题:
(1)通过实验得出该溶液中一定有碳酸钠、氢氧化钠,一定没有硫酸钠、氯化钙.
(2)步骤Ⅰ中产生沉淀的化学方程式为Na2CO3+BaCl2═BaCO3↓+2NaCl.
(3)通过上述实验仍无法判断的物质有氯化钠,要证明其是否存在,可采取的操作是取无色溶液少许,加足量稀硝酸充分反应,滴加硝酸银溶液.
分析 根据碳酸钠能和氯化钡反应生成白色的碳酸钡沉淀,碳酸钡能与酸反应生成气体;氯化钡和硫酸钠可以反应生成不溶于水且不溶于酸的白色沉淀;氯化银沉淀也不溶液水和硝酸,要仔细分析每一实验步骤的用意及实验中所发生的化学反应,从而做出正确的判断.
解答 解:(1)取无色溶液少量,滴加过量氯化钡溶液,过滤,得白色滤渣和无色滤液,说明溶液中存在能与氯化钡反应生成沉淀的碳酸钠或硫酸钠;向步骤Ⅰ所得白色滤渣中加入足量稀硝酸,沉淀全部消失,说明一定没有硫酸钠,因为硫酸钡沉淀不溶于稀硝酸,从而说明溶液中一定不含氯化钙,因为氯化钙可与碳酸钠反应,二者不能共存,0到b点无气体生成,原溶液是碳酸钠和氢氧化钠的混合物,因此原溶液还有氢氧化钠;
(2)步骤Ⅰ中产生沉淀的化学反应是碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,化学方程式是:Na2CO3+BaCl2═BaCO3↓+2NaCl;
(3)向步骤Ⅰ所得无色滤液中加入足量稀硝酸和硝酸银溶液,产生白色沉淀,说明滤液中含有氯离子,由于碳酸钠和氯化钡反应生成氯化钠,无法确定原溶液中是否含有氯化钠;通过上述实验和现象,还无法确定是否含有氢氧化钠,要证氯化钠存在,可取无色溶液少许,加足量稀硝酸充分反应,滴加硝酸银溶液,若仍有沉淀生成,说明含有氯化钠;
故答案为:(1)碳酸钠、氢氧化钠,硫酸钠、氯化钙;
(2)Na2CO3+BaCl2═BaCO3↓+2NaCl;
(3)氯化钠;
取无色溶液少许,加足量稀硝酸充分反应,滴加硝酸银溶液.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.如表为氯化钠和氯化铵在不同温度时的溶解度,回答下列问题:
(1)由表中数据可知,溶解度随温度变化较大的物质是氯化铵.
(2)20℃时100g水最多只能溶解NaCl36g.
(3)向烧杯中加入100g水和50.0g氯化铵配成50℃的溶液,再冷却到20℃,烧杯中析出固体为12.8g.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
| NH4Cl溶解度 | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
| NaCl溶解度 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
(2)20℃时100g水最多只能溶解NaCl36g.
(3)向烧杯中加入100g水和50.0g氯化铵配成50℃的溶液,再冷却到20℃,烧杯中析出固体为12.8g.
13.分别将下列各组物质同时加到水中,能大量共存的是( )
| A. | NaCl AgNO3 | B. | Na2CO3 H2SO4 | C. | CaCl2 Na2CO3 | D. | BaCl2 KOH |
20.在日常生活中,下列说法正确的是( )
| A. | 利用汽油的乳化作用,可以把衣物上的油污洗去 | |
| B. | 包装食品的聚乙烯塑料袋可用加热的方法封口 | |
| C. | 冬天室内用煤炉取暖,为防止煤气中毒,在煤炉上放一盆水 | |
| D. | 空气中的其他成分都分离出去,只留下氧气,对人类的生存更有宜 |
14.下列事实不能用金属的活动性顺序加以解释的是( )
| A. | 不能用铜与稀硫酸反应制取氢气 | |
| B. | 在化合物中,铁显+2、+3价,铜显+1、+2价 | |
| C. | 铁能置换出硫酸铜溶液中的铜 | |
| D. | 同条件下,锌、铁与稀硫酸反应的剧烈程度不同 |
15.化学实验中处处表现出颜色变化美.下列化学实验中的颜色变化不符合实验事实的是( )
| A. | 氢氧化钠溶液中滴入石蕊试液,溶液由无色变蓝色 | |
| B. | 铁钉放入硫酸铜溶液中,溶液由蓝色变为浅绿色 | |
| C. | 氢气在空气中燃烧,发出淡蓝色火焰 | |
| D. | 加热玻璃管中的铜粉,固体由红色变成黑色 |
 化学与生活密切相关.请根据所学知识回答下列问题:
化学与生活密切相关.请根据所学知识回答下列问题: