题目内容
4.称取12.5g石灰石(主要成分是CaCO3,杂质不参加反应且杂质中不含钙元素)放入烧杯中,向其中加入50g稀盐酸,二者恰好完全反应.反应结束后称量烧杯中剩余物质的总质量为58.1g(不包括烧杯的质量,且气体的溶解忽略不计).求:(1)生成二氧化碳的质量.
(2)12.5g石灰石中含钙元素的质量.
(3)稀盐酸中氯化氢气体的质量分数?
分析 碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,根据提供的数据可以进行相关方面的计算.
解答 解:(1)反应前后的质量差即为反应生成二氧化碳的质量,生成二氧化碳质量为:12.5g+50g-58.1g=4.4g,
答:生成了4.4g二氧化碳.
(2)设碳酸钙质量为x,稀盐酸中氯化氢质量为y,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 73 44
x y 4.4g
$\frac{100}{x}$=$\frac{73}{y}$=$\frac{44}{4.4g}$,
x=10g,y=7.3g,
12.5g石灰石中含钙元素的质量为:10g×$\frac{40}{100}$×100%=4g,
答:12.5g石灰石中含钙元素的质量是4g.
(3)稀盐酸中氯化氢气体的质量分数为:$\frac{7.3g}{50g}$×100%=14.6%,
答:稀盐酸中氯化氢气体的质量分数为14.6%.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

练习册系列答案
相关题目
14.下列物质露置在空气中一段时间后,质量变大且变质的是( )
①浓盐酸 ②浓硫酸 ③烧碱 ④食盐 ⑤熟石灰 ⑥铁丝.
①浓盐酸 ②浓硫酸 ③烧碱 ④食盐 ⑤熟石灰 ⑥铁丝.
| A. | ②③⑤ | B. | ②③④ | C. | ③⑤⑥ | D. | ①③⑥ |
15.下列关于化学反应xA+yB═mC+nD(x、y、m、n为化学计量数)的说法中,一定正确的是( )
| A. | x+y=m+n | |
| B. | A、B、C、D四种物质一定都是化合物 | |
| C. | 参加反应的A和B的质量比等于生成物C和D的质量比 | |
| D. | 若A和B的质量都为a g,充分反应后生成物的总质量小于或等于2a g |
9.下列物质中属于纯净物、化合物、无机化合物、盐、钙盐的是 ( )
| A. | 石灰石 | B. | Ca(OH)2 | C. | CaCO3 | D. | CH4 |
16.如图所示4个坐标图分别表示4个实验过程中某些量的变化,其中正确的是.
| A. |  向盐酸中加入水 | B. |  10 mL 5%的H2O2溶液分解 | ||
| C. |  将饱和石灰水升温 | D. | 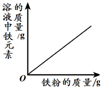 向一定量的稀盐酸中加入铁粉 |
14.新装修的房子不宜立即入住,主要原因是装修材料中发出的甲醛(CH2O)、苯(C6H6)等有害气体对人体可能造成伤害,下列关于这两种有害气体的说法正确的是(相对原子质量:C-12,H-1,O-16)( )
| A. | CH2O与C6H6都属于无机物 | |
| B. | CH2O分子中含有分子 | |
| C. | CH2O中碳的质量分数为40% | |
| D. | C6H6中碳、氢两种元素的质量比为1:1 |

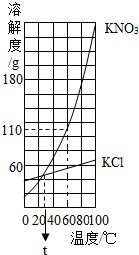 如图是KCl和的溶解度曲线,请回答下列问题:
如图是KCl和的溶解度曲线,请回答下列问题: