题目内容
1.分析下列提供的信息,写出化学方程式.(1)石灰石高温下会分解成两种氧化物CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
(2)加热条件下,一氧化碳与氧化锌反应CO+ZnO$\frac{\underline{\;\;△\;\;}}{\;}$Zn+CO2.
(3)二氧化碳通入澄清石灰水产生沉淀后,继续通二氧化碳,沉淀消失,发生化合反应生成可溶性的Ca(HCO3)2CO2+CaCO3+H2O═Ca (HCO3)2.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:(1)石灰石高温下会分解成生成氧化钙和二氧化碳,反应的化学方程式为CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
(2)加热条件下,一氧化碳与氧化锌反应生成锌和二氧化碳,反应的化学方程式为CO+ZnO$\frac{\underline{\;\;△\;\;}}{\;}$Zn+CO2.
(3)二氧化碳通入澄清石灰水产生沉淀后,继续通二氧化碳,沉淀消失,发生化合反应生成可溶性的Ca(HCO3)2,反应的化学方程式为:CO2+CaCO3+H2O═Ca (HCO3)2.
故答案为:(1)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;(2)CO+ZnO$\frac{\underline{\;\;△\;\;}}{\;}$Zn+CO2;(3)CO2+CaCO3+H2O═Ca (HCO3)2.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
16. 某实验小组在探究金属的化学性质时,得到金属与酸反应制取氢气的质量关系(见图).根据图象信息判断,下列说法正确的是( )
某实验小组在探究金属的化学性质时,得到金属与酸反应制取氢气的质量关系(见图).根据图象信息判断,下列说法正确的是( )
 某实验小组在探究金属的化学性质时,得到金属与酸反应制取氢气的质量关系(见图).根据图象信息判断,下列说法正确的是( )
某实验小组在探究金属的化学性质时,得到金属与酸反应制取氢气的质量关系(见图).根据图象信息判断,下列说法正确的是( )| A. | 四种金属与酸反应的速率:Al>Mg>Fe>Zn | |
| B. | 四种金属的活动性顺序:Mg>Al>Zn>Fe | |
| C. | Al、Mg、Fe、Zn四种金属与酸反应得到氢气的质量比:$\frac{1}{27}$:$\frac{1}{24}$:$\frac{1}{56}$:$\frac{1}{65}$ | |
| D. | 同质量的四种金属与足量酸反应得到氢气的质量:Al>Mg>Fe>Zn |
5.以下物质的性质和用途对应关系不正确的是( )
| A. | 氧气能支持燃烧,所以氧气可作燃料 | |
| B. | 氮气的化学性质不活泼,所以氮气可作保护气 | |
| C. | 镁带燃烧时能发出耀眼的白光,所以镁带可作照明弹 | |
| D. | 石灰水通入二氧化碳可变浑浊,所以石灰水可用于检验二氧化碳 |
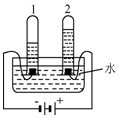 为了探究水的组成,化学兴趣小组的同学在老师的指导下进行水电解的实验.实验如图所示.
为了探究水的组成,化学兴趣小组的同学在老师的指导下进行水电解的实验.实验如图所示.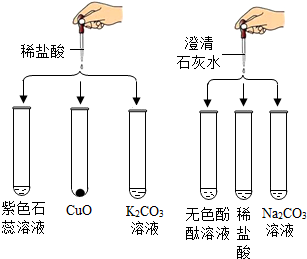 为研究盐酸、氢氧化钙两种物质的化学性质,做了如图所示的6个实验.
为研究盐酸、氢氧化钙两种物质的化学性质,做了如图所示的6个实验.