题目内容
15.信息:①生活垃圾腐烂可产生沼气(主要成分为CH4);焚烧垃圾可产生C02、S02等废气;②S02与C02具有相似的化学性质,都能与碱(如NaOH)反应生成盐和水.阅读上述信息,回答下列问题:
(1)写出沼气燃烧的化学方程式CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)你对焚烧垃圾的意见反对(填“同意”或“反对”),理由是焚烧垃圾会产生有害气体和粉尘,会污染环境,故A符合题意.
分析 (1)根据方程式的写法:一写二配三注明四等号对方程式进行书写;
(2)根据焚烧垃圾会产生有害气体和粉尘进行解答.
解答 解:(1)沼气的主要成分是甲烷,所以沼气燃烧的反应物是甲烷和氧气,生成物是二氧化碳和水,用观察法配平即可,反应条件是点燃.
故答案为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)焚烧垃圾会产生有害气体和粉尘,会污染环境,故A符合题意,故填:反对;焚烧垃圾会产生有害气体和粉尘,会污染环境
点评 环境保护是指人类为解决现实的或潜在的环境问题,协调人类与环境的关系,保障经济社会的持续发展而采取的各种行动的总称.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.下列关于化合物的描述中,正确的是( )
| A. | 由不同元素组成的物质叫化合物 | B. | 由不同元素组成的纯净物叫化合物 | ||
| C. | 由不同原子组成的物质叫化合物 | D. | 由不同分子组成的物质叫化合物 |
6. 化学小组同学取一定量碳酸钙固体高温煅烧一段时间,冷却后,对剩余固体成分进行如下探究.
化学小组同学取一定量碳酸钙固体高温煅烧一段时间,冷却后,对剩余固体成分进行如下探究.
【查阅资料】工业上通常采用高温煅烧石灰石的方法制生石灰,化学方程式为:
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
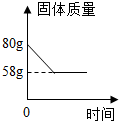
该化学小组取80g的固体样品煅烧(杂质质量无变化),煅烧过程中固体质量变化如图所示,求:①碳酸钙中钙元素的质量分数为40%;
②该石灰石样品中碳酸钙的纯度.
【提出问题】煅烧后剩余固体成分是什么?
【猜想与假设】剩余固体成分:
I.全部是氧化钙Ⅱ.氧化钙和碳酸钙Ⅲ.全部是碳酸钙
在老师指导下,小组同学设计如下实验,探究上述猜想是否成立.
【进行实验】
①甲同学取一定量的剩余固体于试管中,加入一定量的水振荡,有白色不溶物.甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅲ成立.乙同学认为上述实验不足以证明猜想Ⅲ成立,其理由是氧化钙与水反应生成的氢氧化钙微溶于水,也可能出现白色不溶物.
②乙同学取一定量的剩余固体于试管中,加入一定量的水,触摸试管外壁感觉发热,继续向试管中加入几滴稀盐酸,没有气泡产生.乙同学据此认为试管中的固体只有氧化钙,即猜想I成立.丙同学认为乙的实验不足以证明猜想I成立,理由是即使有碳酸钙,加入的少量稀盐酸先消耗氢氧化钙,也不会出现气泡.
③丙同学利用水、无色酚酞溶液和稀盐酸证明了猜想Ⅱ成立,请完成实验报告.
【反思拓展】工业制生石灰的过程中同时得到副产品二氧化碳.下列用途是利用二氧化碳化学性质的是ACD.
A.气体肥料 B.制干冰 C.制纯碱 D.制碳酸饮料.
 化学小组同学取一定量碳酸钙固体高温煅烧一段时间,冷却后,对剩余固体成分进行如下探究.
化学小组同学取一定量碳酸钙固体高温煅烧一段时间,冷却后,对剩余固体成分进行如下探究.【查阅资料】工业上通常采用高温煅烧石灰石的方法制生石灰,化学方程式为:
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
该化学小组取80g的固体样品煅烧(杂质质量无变化),煅烧过程中固体质量变化如图所示,求:①碳酸钙中钙元素的质量分数为40%;
②该石灰石样品中碳酸钙的纯度.
【提出问题】煅烧后剩余固体成分是什么?
【猜想与假设】剩余固体成分:
I.全部是氧化钙Ⅱ.氧化钙和碳酸钙Ⅲ.全部是碳酸钙
在老师指导下,小组同学设计如下实验,探究上述猜想是否成立.
【进行实验】
①甲同学取一定量的剩余固体于试管中,加入一定量的水振荡,有白色不溶物.甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅲ成立.乙同学认为上述实验不足以证明猜想Ⅲ成立,其理由是氧化钙与水反应生成的氢氧化钙微溶于水,也可能出现白色不溶物.
②乙同学取一定量的剩余固体于试管中,加入一定量的水,触摸试管外壁感觉发热,继续向试管中加入几滴稀盐酸,没有气泡产生.乙同学据此认为试管中的固体只有氧化钙,即猜想I成立.丙同学认为乙的实验不足以证明猜想I成立,理由是即使有碳酸钙,加入的少量稀盐酸先消耗氢氧化钙,也不会出现气泡.
③丙同学利用水、无色酚酞溶液和稀盐酸证明了猜想Ⅱ成立,请完成实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量剩余固体于试管中,加水 振荡,过滤 取滤液滴加无色酚酞溶液 取滤渣滴加足量的稀盐酸 | 溶液变红 有气泡产生 | 猜想Ⅱ成立 |
A.气体肥料 B.制干冰 C.制纯碱 D.制碳酸饮料.