题目内容
16. 如图是某化学反应的微观示意图,从图中获得的有关信息正确的是A.
如图是某化学反应的微观示意图,从图中获得的有关信息正确的是A.A.参加反应的
 和
和 的分子个数比为2:1
的分子个数比为2:1B.该化学反应前后分子的个数不变
C.该化学反应中共有三种单质
D.该反应的本质是分子发生再分,原子重新组合.
分析 观察分析化学反应的微观模拟示意图.分析物质的微观构成,判断物质的类别,根据反应的特点分析反应的类型等.
解答 解:A、由物质的微观构成可知,参加反应的 和
和 的分子个数比为2:1.故A正确;
的分子个数比为2:1.故A正确;
B、由化学反应的微观模拟示意图可知,该化学反应前后分子的个数改变.故B错误;
C、由反应前后微粒的变化可知,该化学反应中共有两种单质.故C错误.
D、由化学反应的微观模拟示意图可知,该反应的本质是分子发生再分,原子重新组合.
故选A,D补充:该反应是分子发生再分,原子重新组合.
点评 准确理解化学反应的微观模拟示意图的意义,能分清分子的构成、分子、原子的变化特点等是解决此类题目的关键.

练习册系列答案
相关题目
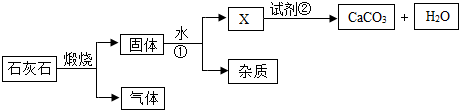
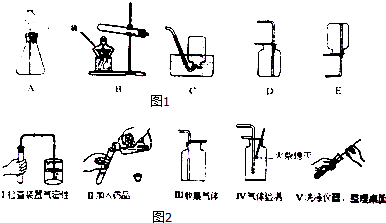
5. 某校化学兴趣小组为了解碳酸氢钠粉末(NaHCO3)的化学性质,进行了如下探究.该小组成员将少量碳酸氢钠粉末置于如图装置的试管中,充分加热至反应完全,发现试管口出现无色液体,澄清石灰水变浑浊,且试管底部有白色固体残余.两位同学提出以下猜想:
某校化学兴趣小组为了解碳酸氢钠粉末(NaHCO3)的化学性质,进行了如下探究.该小组成员将少量碳酸氢钠粉末置于如图装置的试管中,充分加热至反应完全,发现试管口出现无色液体,澄清石灰水变浑浊,且试管底部有白色固体残余.两位同学提出以下猜想:
(1)提出问题:残余白色固体的成分是什么?
(2)猜想与假设:根据化学反应前后元素种类不变,两位同学提出以下猜想:
【猜想一】甲同学:“白色固体是氢氧化钠(NaOH)”;
【猜想二】乙同学:“白色固体是碳酸钠(Na2CO3)”.
(3)实验与结论:①澄清石灰水变浑浊的反应方程式:CO2+Ca(OH)2═CaCO3↓+H2O;
②为了验证自己的猜想,甲同学设计了以下方案并实验验证:
根据甲同学的猜想与验证,乙同学认为甲的结论不准确,因为NaOH与Na2CO3的水溶液均显碱性,都能使无色酚酞试液变红.
③以下是乙同学设计的实验:
④根据以上实验探究内容,写出碳酸氢钠受热分解的化学方程式:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(4)讨论交流:你还能设计不同的实验方案来验证乙同学的猜想吗?
 某校化学兴趣小组为了解碳酸氢钠粉末(NaHCO3)的化学性质,进行了如下探究.该小组成员将少量碳酸氢钠粉末置于如图装置的试管中,充分加热至反应完全,发现试管口出现无色液体,澄清石灰水变浑浊,且试管底部有白色固体残余.两位同学提出以下猜想:
某校化学兴趣小组为了解碳酸氢钠粉末(NaHCO3)的化学性质,进行了如下探究.该小组成员将少量碳酸氢钠粉末置于如图装置的试管中,充分加热至反应完全,发现试管口出现无色液体,澄清石灰水变浑浊,且试管底部有白色固体残余.两位同学提出以下猜想:(1)提出问题:残余白色固体的成分是什么?
(2)猜想与假设:根据化学反应前后元素种类不变,两位同学提出以下猜想:
【猜想一】甲同学:“白色固体是氢氧化钠(NaOH)”;
【猜想二】乙同学:“白色固体是碳酸钠(Na2CO3)”.
(3)实验与结论:①澄清石灰水变浑浊的反应方程式:CO2+Ca(OH)2═CaCO3↓+H2O;
②为了验证自己的猜想,甲同学设计了以下方案并实验验证:
| 实验步骤 | 现象 | 实验结论 |
| 取少量残余固体于试管中,加入适量的水使之溶解,往试管中滴加2滴无色酚酞溶液,观察现象 | 溶液变红 | 白色固体是氢氧化钠 |
③以下是乙同学设计的实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量残余固体于试管中, 加入适量稀盐酸,观察现象 | 试管中产生大量气泡 | 白色固体是碳酸钠 |
(4)讨论交流:你还能设计不同的实验方案来验证乙同学的猜想吗?
| 实验步骤 | 现象 | 实验结论 |
| 白色固体是碳酸钠 |
4.下列变化属于化学变化的是( )
| A. | 高粱发酵制酒精 | B. | 二氧化碳压缩成干冰 | ||
| C. | 木材制成桌椅 | D. | 蒸发海水制得食盐 |
11.镍氢充电电池有着广泛应用,镍及其化合物能发生下列反应:①Ni+2HCl═NiCl2+H2↑;②NiO+2HCl═NiCl2+H2O;③NiO2+4HCl═NiCl2+Cl2↑+2H2O,Ni(OH)2不溶于水,下列有关说法错误的是( )
| A. | 镍的金属活动性比铜强 | |
| B. | 反应②和③都是复分解反应 | |
| C. | NiCl2能与NaOH溶液发生复分解反应 | |
| D. | 反应①、③中的Ni化合价都发生了变化 |
1.根据表中数据,回答下列问题:
(1)若要比较KNO3和NaCl在水中的溶解能力,需要控制水的质量和温度均相同.
(2)30℃时,各取4.5%KNO3固体和NaCl固体,分别加入到10g水中,充分溶解后,达到饱和状态的是NaCl溶解,该温度下,不能(选填“能”或“不能”)配制出45.8%的KNO3的溶液.
(3)根据上表提供的数据可绘制出KNO3和NaCl的溶解度曲线,两条曲线的交点所在的温度范围是B(填序号).
A.大于0℃,小于10℃B.大于20℃,小于30℃
C.大于40℃,小于50℃D.大于60℃,小于70℃
(4)将20℃时KNO3和NaCl的饱和溶液升温到80℃(不考虑水分的蒸发),溶质量分数NaCl溶液.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | |
| 溶解度/g | KNO3 | 13.3 | 20.5 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 | |
(2)30℃时,各取4.5%KNO3固体和NaCl固体,分别加入到10g水中,充分溶解后,达到饱和状态的是NaCl溶解,该温度下,不能(选填“能”或“不能”)配制出45.8%的KNO3的溶液.
(3)根据上表提供的数据可绘制出KNO3和NaCl的溶解度曲线,两条曲线的交点所在的温度范围是B(填序号).
A.大于0℃,小于10℃B.大于20℃,小于30℃
C.大于40℃,小于50℃D.大于60℃,小于70℃
(4)将20℃时KNO3和NaCl的饱和溶液升温到80℃(不考虑水分的蒸发),溶质量分数NaCl溶液.
6.逻辑推理是化学学习中常用的思维方法.下列推理正确的是( )
| A. | 中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| B. | 化合物都是由不同种元素组成的,所以不同种元素组成的纯净物一定是化合物 | |
| C. | 置换反应中有单质生成,所以有单质生成的反应一定属于置换反应 | |
| D. | 燃烧伴有发光、放热现象,所以有发光、放热的现象就一定是燃烧 |