题目内容
4.根据如图甲的装置图回答问题: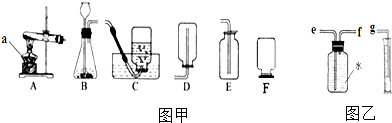
(1)写出图甲中标有a的仪器名称:a酒精灯.
(2)用高锰酸钾制取较纯净氧气应选择的装置组合为AC(填序号),写出该反应的符号表达式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,收集到的气体呈紫红色的原因是试管口没有塞一团棉花.
(3)若选用B和C装置制取氧气,写出实验室利用该套装置制取氧气的符号表达式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,小倪用如图乙装置收集并测量氧气的体积,其中量筒的作用是测量排出水的体积,该装置导管的连接顺序是e接g(填接口编号)
(4)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,发生装置可选择A(填序号).甲烷气体一般采用装置C进行收集,收集满后集气瓶的放置方式如装置F所示,据此推断甲烷具备的物理性质是:密度比空气小(任写一条).
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
为了防止高锰酸钾进入导管,通常在试管口塞一团棉花;
氧气的密度比空气的密度大,不易溶于水;
(3)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(4)根据收集气体的方法可以判断气体的性质.
解答 解:(1)标有a的仪器名称是酒精灯,常用作热源.
故填:酒精灯.
(2)用高锰酸钾制取氧气需要加热,应该用A装置作为发生装置;
因为氧气的密度比空气大,可以用向上排空气法收集,即用E装置收集,氧气不易溶于水,可以用排水法收集,即用C装置收集,用排水法收集的氧气比用排空气法收集的氧气纯净;
该反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
收集到的气体呈紫红色的原因是试管口没有塞一团棉花.
故填:AC;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;试管口没有塞一团棉花.
(3)若选用B和C装置制取氧气不需要加热,应该是利用过氧化氢和二氧化锰制取氧气,过氧化氢分解的化学方程式为:;
用如图乙装置收集并测量氧气的体积,其中量筒的作用是测量排出水的体积,生成氧气的体积即为排出水的体积,该装置导管的连接顺序是e接g.
故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;测量排出水的体积;e.
(4)用无水醋酸钠和碱石灰的混合固体制取甲烷气体需要加热,发生装置应该用A;
甲烷气体一般采用装置C进行收集,说明甲烷不溶于水,收集满后集气瓶的放置方式如装置F所示,说明甲烷的密度比空气小.
故填:A;密度比空气小.
点评 本题主要考查仪器的用途、反应表达式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.

 阅读快车系列答案
阅读快车系列答案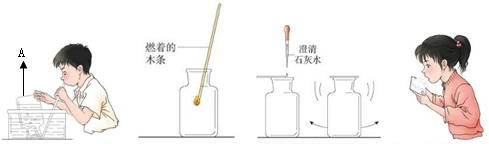
(1)先用排水法收集两瓶呼出气体,仪器A的用途是收集或贮存少量气体.
(2)请你将主要实验操作、现象和结论以文字的形式填入下列表格中的横线部分:
| 探究目的 | 实验操作 | 实验现象 | 实验结论 |
| 比较吸入的空气与呼出气体中氧气含量的区别 | 将两根燃着的小木条分别插入空气样品和呼出气体的样品 | 空气样品中的小木条 正常燃烧 呼出气体的样品中的小木条很快熄灭 | 空气样品中氧气的含量比呼出气体中的氧气含量高 |
| 比较吸入的空气与呼出气体中二氧化碳含量的区别 | 向一瓶空气样品和一瓶呼出气体的样品中滴入相同滴数的澄清石灰水 | 空气样品中的澄清石灰水无明显变化 呼出气体的样品中的澄清石灰水变白色浑浊 | 空气样品中二氧化碳的含量比呼出气体中的二氧化碳含量低 |
| 比较吸入的空气与呼出气体中水蒸气含量的区别 | 取两块干燥的玻璃片,对着其中一片哈气,将另一块玻璃片放置在空气中 | 对着哈气的玻璃片上出现水雾 另一块玻璃片无明显变化 | 空气样品中水蒸气的含量比呼出气体中的水蒸气含量低 |
 5月7日天津宏迪工程检测发展有限公司在进行探伤作业期间,丢失了用于探伤的放射源铱-192一枚.铱-192除可用于工业中的无损探伤外,还可用于治疗癌症.如图是元素周期表中关于铱元素的信息.下列关于铱元素的说法错误的是( )
5月7日天津宏迪工程检测发展有限公司在进行探伤作业期间,丢失了用于探伤的放射源铱-192一枚.铱-192除可用于工业中的无损探伤外,还可用于治疗癌症.如图是元素周期表中关于铱元素的信息.下列关于铱元素的说法错误的是( )| A. | 铱元素属于非金属元素 | B. | 相对原子质量为192.2 | ||
| C. | 原子核外有77个电子 | D. | 铱的原子序数为77 |
| A. | 1个硫化丙烯分子中含有3个氢分子 | |
| B. | 硫化丙烯由3个碳原子、6个氢原子、1个硫原子构成 | |
| C. | 硫化丙烯是由碳、氢、硫三种元素组成的化合物 | |
| D. | 硫化丙烯中C、H、S元素原子质量比为3:6:1 |
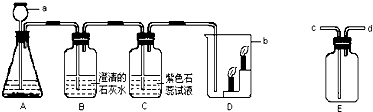
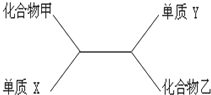 根据下列化合物与单质相互转化的关系回答:
根据下列化合物与单质相互转化的关系回答:
