题目内容
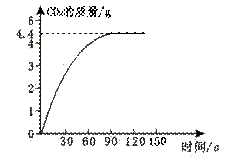 某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁,他们为了测定水垢中碳酸钙的含量,取某种稀盐酸100 g加入到15.8 g水垢中,产生CO2气体的情况如下图所示。计算:
某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁,他们为了测定水垢中碳酸钙的含量,取某种稀盐酸100 g加入到15.8 g水垢中,产生CO2气体的情况如下图所示。计算:
(1)从图中可以看出15.8 g水垢与盐酸反应后
生成CO2最多是 。
(2)水垢中碳酸钙的质量分数是多少?(计算
结果保留0.1%)
(3)所用稀盐酸中溶质质量分数是多少?(计算结果保留0.1%)
考点:
根据化学反应方程式的计算;有关溶质质量分数的简单计算..
专题:
综合计算(图像型、表格型、情景型计算题).
分析:
由表中数据可以判断生成二氧化碳的质量,根据二氧化碳的质量可以计算碳酸钙的质量、稀盐酸中氯化氢的质量,进一步可以计算水垢中碳酸钙的质量分数和所用稀盐酸中溶质的质量分数.
解答:
解:(1)从图中可以看出15.8g水垢与盐酸反应后生成CO2最多是4.4g.
故填:4.4g.
(2)设碳酸钙的质量为x,氯化氢的质量为y,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 73 44
x y 4.4g
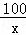 =
=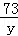 =
=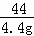 ,
,
x=10g,y=7.3g,
水垢中碳酸钙的质量分数是: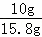 ×100%=63.3%,
×100%=63.3%,
答:水垢中碳酸钙的质量分数是63.3%.
(3)所用稀盐酸中溶质质量分数是: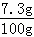 ×100%=7.3%,
×100%=7.3%,
答:所用稀盐酸中溶质质量分数是7.3%.
点评:
本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

除去下列物质中的少量杂质,所选用的试剂及反应类型均正确的是
| 选项 | 物质(括号内为杂质) | 试剂 | 反应类型 |
| A | CO2(CO) | 足量 CuO | 化合反应 |
| B | CuO(Cu) | 足量 O2 | 置换反应 |
| C | H2O(H2O2) | 足量 MnO2 | 分解反应 |
| D | Ca(OH)2(CaO) | 适量稀盐酸 | 复分解反应 |
A.A B.B C.C D.D
小强在一 次查阅资料时得知:二氧化碳与氢氧化钠反应,若二氧化碳过量,生成的碳酸钠会继续与二氧化碳反应生成碳酸氢钠,反应原理为:Na2CO3+CO2+H2O=2NaHCO3.出于好奇,他和同学一起向一定量的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后,低温蒸发结晶,得到了白色固体.
次查阅资料时得知:二氧化碳与氢氧化钠反应,若二氧化碳过量,生成的碳酸钠会继续与二氧化碳反应生成碳酸氢钠,反应原理为:Na2CO3+CO2+H2O=2NaHCO3.出于好奇,他和同学一起向一定量的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后,低温蒸发结晶,得到了白色固体.
【提出问题】白色固体是什么?
【作出猜想】
猜想Ⅰ:只有Na2CO3;
猜想Ⅱ:可能是Na2CO3和NaOH的混合物;
猜想Ⅲ: _________
【査阅资料】
(1)碳酸氢钠不稳定受热易分解2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
(2)Na2CO3与NaOH的热稳定性较好
(3)CaCl2和NaCl的水溶液呈中性
【设计实验】
取一定量的白色固体,加热,若固体质量不变,猜想 _________ 错误;若固体质量减少,则二氧化碳与氢氧化钠反应后, _________ 过量.
【交流讨论】
小方认为,要想知道白色固体中是否有氢氧化钠,可将白色固体配成溶液后,直接用pH试纸测试即可作出判断,你认为是否可行? _________ ;理由是 _________ .
【继续探究】白色固体中是否有氢氧化钠?
| 实验操作 | 实验现象 | 目的/结论 |
| ①取白色固体适量配制成溶液.往所得溶液中滴加过量的 _________ ,充分反应后,过滤. | 有白色沉淀生成 | 除去白色固体中的 _________ |
| ②取滤液,往滤液中滴入几滴 _________ | _________ | 白色固体中没有氢氧化钠 |
【交流与反思】
由于氢氧化钠能与二氧化碳反应,所以实验室保存氢氧化钠一定要注意 _________ .
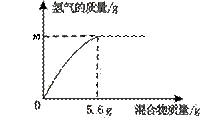 (4)现有两种金属单质组成的混合物。向100 g某稀盐酸中加入该混合物,混合物的质量与生成氢气的质量关系如图所示。
(4)现有两种金属单质组成的混合物。向100 g某稀盐酸中加入该混合物,混合物的质量与生成氢气的质量关系如图所示。 A. 10g水与10g酒精混合,得到20g液体,这个过程符合质量守恒定律
A. 10g水与10g酒精混合,得到20g液体,这个过程符合质量守恒定律