题目内容
10.下列各组离子在无色溶液中能大量共存的是( )| A. | Ag+、K+、NO3-、Cl- | B. | Na+、Ba2+、NO3-、OH- | ||
| C. | Cu2+、Mg2+、Cl-、NO3- | D. | H+、Ca2+、CO32-、OH- |
分析 本题利用复分解反应的条件来判断物质能否共存的问题,若物质在水中解离成的离子重新结合生成水或气体或沉淀时,物质就不能共存.本题还要注意能得到无色透明溶液,则应注意常见离子在水中的颜色.
解答 解:A、银离子和氯离子反应生成氯化银白色沉淀,不能大量共存,故选项错误;
B、四者之间不反应,能大量共存,且不存在有色离子,故选项正确;
C、铜离子为蓝色溶液,故选项错误;
D、氢离子和碳酸根离子结合产生水和二氧化碳,和氢氧根离子结合产生水,碳酸根离子和钙离子结合产生碳酸钙沉淀,不能大量共存,故选项错误;
故选项为:B.
点评 本题考查物质的共存问题,判断物质在溶液中能否共存,主要看溶液中的各物质之间能否发生反应生成沉淀、气体、水;还要注意特定离子的颜色.

练习册系列答案
相关题目
1.现含有HCl和氯化铜的混合溶液50g,将160g溶质的质量分数为10%的氢氧化钠溶液平均分四次加入到该混合液中,生成沉淀的质量与加入氢氧化钠的溶液的质量关系如表.
(1)第四次加入氢氧化钠,溶液中的溶质有NaCl、NaOH;(填化学式)
(2)求混合溶液中氯化铜的质量分数.(写出计算过程)
(3)画出在该混合溶液中加入氢氧化钠溶液质量与生成沉淀质量变化关系的曲线(请在答题卷上面,并标出折点坐标)
| 次数 | 1 | 2 | 3 | 4 |
| 加入氢氧化钠溶液的质量合计/g | 40 | 80 | 120 | 160 |
| 生成的沉淀质量/g | 0 | 4.9 | 9.8 | 9.8 |
(2)求混合溶液中氯化铜的质量分数.(写出计算过程)
(3)画出在该混合溶液中加入氢氧化钠溶液质量与生成沉淀质量变化关系的曲线(请在答题卷上面,并标出折点坐标)
5.下列符号中,既具有宏观意义,又具有微观意义的是( )
| A. | 2O | B. | O2 | C. | 2H2O | D. | 2O2- |
15.如图实验装置进行的相应实验,达不到实验目的是( )
| A. |  用如图所示装置除去CO2中含有的少量HCl气体 | |
| B. | 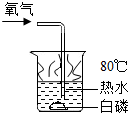 用如图所示的装置证明可燃物燃烧需要与氧气接触 | |
| C. | 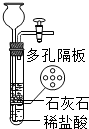 用如图所示装置制取少量CO2气体 | |
| D. |  在实验室中,用如图所示装置除去少量黄河水中的泥沙 |
2.用分子的知识解释下列现象,正确的是( )
| A. | 带火星的木条在氧气中能复燃,在空气中却不能,说明它们中氧分子的化学性质不同 | |
| B. | 缉毒犬根据气味发现毒品,是由于分子不断运动 | |
| C. | 降温能使水结成冰,是因为低温下水分子静止不动 | |
| D. | 变瘪的乒乓球放入热水中能鼓起来,是由于分子受热体积变大 |
 化学与生活、生产关系密切.请回答下列问题:
化学与生活、生产关系密切.请回答下列问题: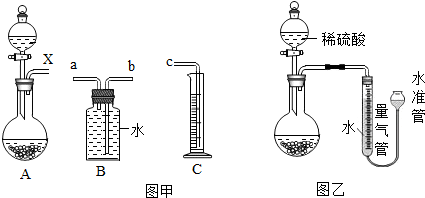
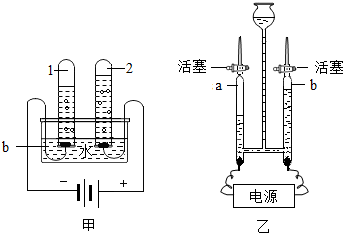 如图,甲、乙两图都是电解水的简易装置.回答下列问题.
如图,甲、乙两图都是电解水的简易装置.回答下列问题.