题目内容
14.(1)N(NO2)3是科学家2011年发现的一种新型火箭燃料,其中氮元素和氧元素的质量比为7:12.(2)尿素CO(NH2)2是常见化肥中含氮量最高的氮肥,则氮元素质量分数为46.7%.(结果保留一位小数)
(3)小刚用盐酸溶液,验证了Mg、Fe、Cu、Ag四种金属的活动性顺序是依次减弱的,能说明Mg比Fe活泼的实验现象是镁与稀盐酸反应速度比铁与稀盐酸反应速度快;能说明Fe比Cu活泼的实验现象是铁丝的表面有红色的物质生成.
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
(3)在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,据此进行分析解答.
解答 解:(1)N(NO2)3中氮元素和氧元素的质量比为(14×4):(16×2×3)=7:12.
(2)尿素中氮元素质量分数为$\frac{14×2}{12+16+(14+1×2)×2}$×100%≈46.7%.
(3)由金属活动性顺序表可知,运用稀盐酸首先可验证镁比铁活泼,镁、铁比铜、银活泼.因为稀盐酸和铁镁能反应生成氢气,而铜银与稀盐酸不反应不产生氢气,且镁比铁产生氢气的速度快.但不能验证铜和银的金属活动性.
利用金属活动顺序表中前面的金属能把后面的金属从它的化合物的溶液中置换出来,可用硫酸铜溶液来比较铁、铜的活动性.
说明Mg比Fe活泼的实验现象是:镁与稀盐酸反应速度比铁与稀盐酸反应速度快;
说明Fe比Cu活泼的实验现象是:将铁丝放入硫酸铜溶液中,铁丝的表面有红色的物质生成.
故答案为:(1)7:12;(2)46.7%;(3)镁与稀盐酸反应速度比铁与稀盐酸反应速度快;铁丝的表面有红色的物质生成.
点评 本题难度不大,灵活运用化学式的有关计算、掌握金属活动性顺序并能灵活运用是正确解答本题的关键所在.

练习册系列答案
相关题目
19.下列各种物质中.由原子直接构成的是( )
| A. | 金刚石 | B. | 氮气 | C. | 食盐 | D. | 二氧化硫气体 |
5.为提纯下列物质,所选用的除杂试剂和操作方法都正确的是( )
| 序号 | 物质(括号内为杂质) | 除杂试剂 | 操作方法 |
| A | 氧气(二氧化碳) | 木炭 | 通过灼热的木炭 |
| B | 氯化铜溶液(氯化锌) | 金属铜 | 过滤 |
| C | 二氧化碳(一氧化碳) | 氢氧化钠溶液 | 洗气 |
| D | 铜粉(氧化铜粉末) | 稀盐酸 | 过滤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
6.下列物质与对应的化学式书写错误的是( )
| A. | 氯化钠NaCl | B. | 二氧化碳 CO2 | C. | 碳酸钠 NaCO3 | D. | 四氧化三铁Fe3O4 |
3.下列说法正确的是( )
| A. | 某物质只含有一种元素,则该物质一定是单质 | |
| B. | 中和反应一定有盐和水生成 | |
| C. | 固体物质的溶解度都随温度的升高而增大 | |
| D. | 溶液都是无色透明的 |
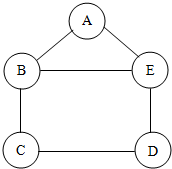 小吴用铁、硫酸、氢氧化钡、硫酸铜和碳酸钠五中物质玩化学拼图游戏(如图),游戏规则要求图中相邻物质之间能发生反应.其中C的溶液呈蓝色,
小吴用铁、硫酸、氢氧化钡、硫酸铜和碳酸钠五中物质玩化学拼图游戏(如图),游戏规则要求图中相邻物质之间能发生反应.其中C的溶液呈蓝色,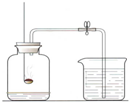 某课外小组设计了测定空气中氧气含量的实验,按下图进行实验:
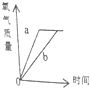
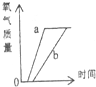
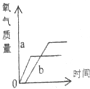
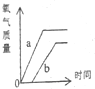
某课外小组设计了测定空气中氧气含量的实验,按下图进行实验: