题目内容
称取某石灰石样品20g在高温条件下充分煅烧(杂质不反应),称得剩余固体为13.4g,求该石灰石样品中CaCO3的质量分数.(提示:石灰石的主要成分为碳酸钙,碳酸钙高温分解的化学方程式为CaCO3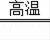
 CaO+CO2↑ )
CaO+CO2↑ )
【考点】根据化学反应方程式的计算.
【专题】有关化学方程式的计算;有关化学方程式的计算.
【分析】根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.由碳酸钙高温煅烧的化学方程式可知生成的二氧化碳的质量=反应前各物质的质量总和﹣反应后剩余固体的质量;并据生成二氧化碳的质量计算出碳酸钙的质量,然后根据质量分数公式计算即可.
【解答】解:完全反应后生成二氧化碳的质量为:20g﹣13.4g=6.6g;
设生成6.6g二氧化碳,需碳酸钙的质量为x.
CaCO3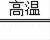
 CaO+CO2↑
CaO+CO2↑
100 44
x 6.6g
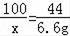

x=15g,
石灰石样品中碳酸钙的质量分数: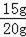
 ×100%=75%.
×100%=75%.
答:石灰石样品中碳酸钙的质量分数为75%.
【点评】本题主要考查学生运用质量守恒定律分析解决问题,及利用化学方程式和质量分数公式进行计算的能力.

 阅读快车系列答案
阅读快车系列答案