题目内容
7. 81岁的宁波籍科学家屠呦呦,登上了国际生物大奖“拉斯克奖”的领奖台,因为她发现了青蒿素,一种用于治疗疟疾的药物,挽救了全球特别是发展中国家是数百人的生命,青蒿素的化学式是C15H22O5,如图是该药说明书中的部分内容,则:
81岁的宁波籍科学家屠呦呦,登上了国际生物大奖“拉斯克奖”的领奖台,因为她发现了青蒿素,一种用于治疗疟疾的药物,挽救了全球特别是发展中国家是数百人的生命,青蒿素的化学式是C15H22O5,如图是该药说明书中的部分内容,则:(1)青蒿素中氢、氧元素的质量比为11:40,碳元素的质量分数为63.83%;
(2)用该药物控制疟疾症状一般三天一个疗程,根据图中提供的“用法与用量”及“剂型与规格”,一个成人在一个疗程中共需服青蒿素几片?25片.
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
(2)根据题意,用该药物控制疟疾症状一般三天一个疗程,根据图中提供的“用法与用量”及“剂型与规格”,首次1.0g,6-8小时后再服0.5g,第2、3日各0.5g,进行分析解答.
解答 解:(1)青蒿素中氢、氧三种元素的质量比为(1×22):(16×5)=11:40.
碳元素的质量分数为$\frac{12×15}{12×15+1×22+16×5}$×100%≈63.83%.
(2)用该药物控制疟疾症状一般三天一个疗程,根据图中提供的“用法与用量”及“剂型与规格”,首次1.0g,6-8小时后再服0.5g,第2、3日各0.5g,则一个成人在一个疗程中共需服用青蒿素的质量为1.0g+0.5g+0.5g×2=2.5g;每片含100mg=0.1g,则一个成人在一个疗程中共需服青蒿素的片数为2.5g÷0.1g/片=25片.
故答案为:(1)11:40;(2)63.83%;(3)25片.
点评 本题难度不大,考查同学们结合标签新信息、灵活运用化学式的有关计算等进行分析问题、解决问题的能力.

练习册系列答案
相关题目
17.早期化学家为了认识空气的本质,将一些物质放在密闭的容器中进行实验,结果发现:每次都有约$\frac{1}{5}$的空气不知去向.当时化学家把这$\frac{1}{5}$的空气称为“有用空气”这种“有用空气”是指( )
| A. | 氮气 | B. | 二氧化碳 | C. | 氧气 | D. | 稀有气体 |
18.如图所示图象能正确反映对应变化关系的是( )
| A. | 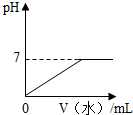 加水稀释一定量氢氧化钠溶液 | |
| B. |  实验室加热氯酸钾制取氧气 | |
| C. | 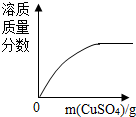 向一定量水中加入硫酸铜固体 | |
| D. | 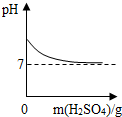 向一定量氢氧化钠溶液中加入稀H2SO4 |
15.现有锌和另一种金属组成的混合物,把6.5g该混合物加入到足量的稀硫酸中,恰好完全反应,产生氢气的质量为w.则下列说法中正确的是( )
| A. | 该混合物可能是Zn、A1,w可能是0.2g | |
| B. | 该混合物可能是Zn、Fe,w可能是0.2g | |
| C. | 若混合物为Zn、Cu,w是0.1g,则该混合物中锌的质量分数为50% | |
| D. | 若混合物为Zn、Mg,w是0.1g,则该混合物中锌的质量分数为50% |