题目内容
14. 向含有CuSO4和HCl的混合溶液中逐滴加入一定量的NaOH溶液,充分反应,生成沉淀的质量(m1)与加入NaOH溶液的质量(m2)的关系如图所示,回答下列问题:
向含有CuSO4和HCl的混合溶液中逐滴加入一定量的NaOH溶液,充分反应,生成沉淀的质量(m1)与加入NaOH溶液的质量(m2)的关系如图所示,回答下列问题:(1)在A点-B点之间,发生反应的化学方程式为CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
(2)B点,过滤,滤液的pH=7.
分析 根据向含有CuSO4和HCl的混合溶液中逐滴加入一定量的NaOH溶液,氢氧化钠会先与盐酸反应,再与硫酸铜反应,然后结合图象的走向进行分析.
解答 解:向含有CuSO4和HCl的混合溶液中逐滴加入一定量的NaOH溶液,氢氧化钠会先与盐酸反应,再与硫酸铜反应,所以
(1)在A点-B点之间,发生的反应是氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,化学方程式为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
(2)B点,沉淀的质量达到了最大值,所以硫酸铜、盐酸和氢氧化钠完全反应,过滤,滤液的pH=7.
故答案为:(1)CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
(2)=.
点评 在解此类题时,首先分析题中图象的变化趋势,然后结合学过的知识进行解答.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
4.已知:草酸钙[CaC2O4]比碳酸钙受热易分解,CaC2O4$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3+CO↑.将12.8gCaC2O4固体加热一段时间后剩余5.6g固体.下列说法正确的是( )
| A. | 剩余固体为混合物 | |
| B. | 剩余固体中含有钙元素的质量为4.0g | |
| C. | 将剩余固体溶于足量水中,其溶质质量为7.6g | |
| D. | 将加热产生的气体全部通入足量澄清石灰水中,生成5.0g固体 |
9.下列对事实的解释中,合理的是( )
| A. | 生铁和钢的性质不同--含碳量不同 | |
| B. | 金刚石和石墨物理性质差异较大--碳原子的排列顺序不同 | |
| C. | 一氧化碳和二氧化碳的性质不同--含有氧原子的个数不同 | |
| D. | 硫在空气和氧气中燃烧的火焰颜色不同--氧气浓度不同导致氧分子的化学性质不同 |
4.下列实验现象的描述中,错误的是( )
| A. | 镁带在空气中燃烧,发出耀眼白光,放热,生成白色固体 | |
| B. | 把铁丝插入硫酸铜溶液中,铁丝表面会覆盖一层红色物质 | |
| C. | 硫在空气中燃烧产生淡蓝色火焰、放热、生成二氧化硫 | |
| D. | 木炭粉与氧化铜粉末混合高温加热,混合物中出现红色物质 |
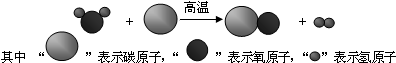




 构建模型和构建知识网络是学习化学重要的学习方法,小军同学利用左手构建酸的化学性质知识网络,如图所示(其中A、B表示与酸反应的
构建模型和构建知识网络是学习化学重要的学习方法,小军同学利用左手构建酸的化学性质知识网络,如图所示(其中A、B表示与酸反应的