题目内容
11.我市正在实施一项宏伟的工程----兴建“海上荣成”,旨在充分开发我市濒临的渤海资源,造福潍纺人民.小明同学住在渤海边上,他对建设“海上潍纺”的宏伟规划很感兴趣.小明模拟化工厂的生产流程,以海水和贝壳(主要成分是碳酸钙)为原料制取生产镁的原料----无水MgCl2.

①试剂a是一种溶液,加入该试剂时发生反应的化学方程式MgCl2+2NaOH=2NaCl+Mg(OH)2↓.
②加入试剂后,要将Mg(OH)2沉淀分离出来,应该应用的方法是过滤,如果在学校实验室中完成该实验,需要的玻璃仪器除烧杯、玻璃棒外还有漏斗.
③流程中的X是“一定条件下,结晶”,在这里应该采用蒸发结晶的方法.
④金属镁是一种较活泼金属,在二氧化碳气体中也能燃烧.燃烧的化学方程式为
2Mg+C02$\frac{\underline{\;点燃\;}}{\;}$C+2MgO,此反应类型属于C
A.分解反应 B.化合反应 C.置换反应 D.复分解反应.
分析 ①、根据生成氢氧化镁沉淀必须在海水中加碱溶液,由贝壳制得的碱只能是氢氧化钙回答a溶液中的溶质;根据氯化镁与氢氧化钙反应生成氯化钙和氢氧化镁沉淀书写方程式;
②、根据过滤的原理和操作过程进行分析回答;
③、根据从氯化镁溶液中得到无水氯化镁,应采用蒸发结晶的方法回答;
④、根据反应的特点分析反应的类型.
解答 解:①、试剂a与海水中的氯化镁反应生成了氢氧化镁沉淀,则试剂a中的溶质一定是一种碱,以贝壳(主要成分是碳酸钙)为原料制取的碱为氢氧化钙,所以试剂a中的溶质是Ca(OH)2;氯化镁与氢氧化钙反应生成氯化钙和氢氧化镁沉淀,故方程式为:MgCl2+Ca(OH)2═CaCl2+Mg(OH)2↓;
②、过滤是分离液体与不溶于液体的固体的方法,所以从液体混合物中提取氢氧化镁沉淀用过滤的方法,如果在学校实验室中完成该实验,需要的玻璃仪器除烧杯、玻璃棒外还有漏斗.
③、从氯化镁溶液中得到无水氯化镁,应采用蒸发的方法,流程中的X是“一定条件下,结晶”,即是蒸发结晶的方法.
④、由化学方程式2Mg+C02$\frac{\underline{\;点燃\;}}{\;}$C+2MgO可知,此反应是一种单质与一种化合物反应生成了另一种单质和另一种化合物,属于置换反应.
故答为:①MgCl2+2NaOH=2NaCl+Mg(OH)2↓;②过滤,漏斗,③蒸发,④C.
点评 海洋是人类巨大的自然宝库,不单是自然界中最大的储水库,还蕴藏着丰富的化学资源.了解过滤的原理和使用仪器,掌握氯化镁、盐酸、氢氧化镁等物质的化学性质是解题的关键点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬.好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,邀请你一同参加.
【知识回放】
金属活动性顺序:K Ca Na Mg Al ZnFeSn Pb(H)CuHg Ag Pt Au,请你在横线上填写对应金属的元素符号.
【作出猜想】
猜想1.Cr>Fe>Cu; 猜想2.Fe>Cu>Cr; 猜想3.你的猜想是Fe>Cr>Cu.
【查阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
【结论与解释】
(1)小聪得到的结论是猜想1正确.
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化物.
【知识运用】
将铬片投入FeSO4溶液中,反应能(填“能”或“不能”)进行.若能进行,请你写出反应的化学方程式Cr+FeSO4=Fe+CrSO4.
【知识回放】
金属活动性顺序:K Ca Na Mg Al ZnFeSn Pb(H)CuHg Ag Pt Au,请你在横线上填写对应金属的元素符号.
【作出猜想】
猜想1.Cr>Fe>Cu; 猜想2.Fe>Cu>Cr; 猜想3.你的猜想是Fe>Cr>Cu.
【查阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验 操作 | 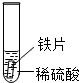 |  | 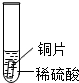 |
| 实验 现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 | 无明显现象 |
(1)小聪得到的结论是猜想1正确.
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化物.
【知识运用】
将铬片投入FeSO4溶液中,反应能(填“能”或“不能”)进行.若能进行,请你写出反应的化学方程式Cr+FeSO4=Fe+CrSO4.
19.下列说法错误的是( )
| A. | 原子的质量几平都集中在原子核上 | |
| B. | 原子通过得失电子形成离子,但离子不能形成原子 | |
| C. | 原子、分子、离子、电子都是构成物质的微粒. | |
| D. | 由分子构成的物质发生化学变化时,分子本身改变 |
16.很多物质都能在氧气中燃烧,下列有关现象的描述正确的是( )
| A. | 硫粉在氧气中燃烧,产生淡蓝色的火焰 | |
| B. | 红磷在氧气中燃烧,产生大量的白雾 | |
| C. | 碳在空气中燃烧,发出耀眼的红光,生成黑色气体 | |
| D. | 铁丝在氧气中燃烧,火星四射,生成黑色固体 |
1.“一带一路”是跨越时空的宏伟构想,赋予古丝绸之路崭新的时代内涵.古丝绸之路将中国的发明和技术传送到国外.下列属于化学变化的是( )
| A. | 罗盘航海 | B. | 火药爆炸 | C. | 蚕丝织衣 | D. | 铁水铸鼎 |
 2015年12月10日,在瑞典斯德哥尔摩,诺贝尔奖颁奖典礼举行,如图为我国女药学家屠呦呦领奖,谱贝尔生理学或医学奖评産委员会主席齐拉特対新华社记者说“中国女科学家屠呦呦从中药中分离出青蒿素应用子疟疾治疗,这表明中国传统的中草药也能给科学家们带来新的启发.”她表示,经过现代技术的提纯和与现代医学相结合,中草药在疾病治疗方面所取得的成就“很了不起”,
2015年12月10日,在瑞典斯德哥尔摩,诺贝尔奖颁奖典礼举行,如图为我国女药学家屠呦呦领奖,谱贝尔生理学或医学奖评産委员会主席齐拉特対新华社记者说“中国女科学家屠呦呦从中药中分离出青蒿素应用子疟疾治疗,这表明中国传统的中草药也能给科学家们带来新的启发.”她表示,经过现代技术的提纯和与现代医学相结合,中草药在疾病治疗方面所取得的成就“很了不起”,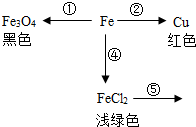 化学使世界变得绚丽多彩.如图是铁与其他物质之间的关系及颜色变化.请写出:
化学使世界变得绚丽多彩.如图是铁与其他物质之间的关系及颜色变化.请写出: