题目内容
18.请回答下列有关金属材料的问题.(1)2017年5月5日运20大型运输机完成了溅水试验,对于肩负中国空军战略运输重任的运20来说,在复杂乃至恶劣野战条件下的跑道运行能力至关重要.运20飞机上运用了大量铝合金材料,下列对铝及其合金的说法不正确的是D.
A.铝具有密度小和抗腐蚀性能
B.铝的导电性好,常用于制作导线
C.铝合金强度和硬度均比纯铝强
D.铝耐腐蚀,故金属活泼性差
(2)下列是与铁的性质有关的部分实验图:
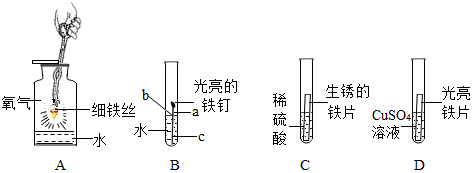
①A中细铁丝燃烧生成的黑色固体物质的化学式是Fe3O4.
②B中铁钉最易生锈的部位是b(填“a”、“b”或“c”).
③C中刚开始无气泡产生,溶液颜色逐渐由无色变为黄色,此时试管内发生反应的化学方程式是Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
④D中反应一段时间后,试管内溶液质量与反应前相比减小(填“增大”、“不变”或“减小”).
(3)在AgNO3、Al(NO3)3、Cu(NO3)2的混合溶液中加入一定量的铜粉,充分反应后过滤,得到溶液甲和固体乙,溶液甲呈蓝色.
①固体乙中一定含有Ag.
②溶液甲中一定含有的阳离子为铝离子和铜离子.
(4)为测定某Cu-Zn合金中铜的质量分数,某同学将10g该合金放入到盛有40g足量稀硫酸的烧杯中,充分反应后,测得烧杯中剩余物质的质量为49.9g,请计算原合金中铜的质量分数.
分析 (1)铝的化学性质比较活泼,通常情况下能和空气中的氧气反应生成氧化铝;
(2)铁在氧气中燃烧生成四氧化三铁;
铁和水、氧气同时接触时容易生锈;
铁锈的主要成分是氧化铁,能和稀硫酸反应生成硫酸铁和水;
④铁和硫酸铜反应生成硫酸亚铁和铜;
(3)铝比铜活泼,铜比银活泼;
(4)铜不能和稀硫酸反应,锌能和稀硫酸反应生成硫酸锌和氢气,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)A.铝具有密度小和抗腐蚀性能,该选项说法正确;
B.铝的导电性好,常用于制作导线,该选项说法正确;
C.铝合金强度和硬度均比纯铝强,该选项说法正确;
D.铝耐腐蚀,是因为铝的化学性质比较活泼,通常情况下能和空气中的氧气反应生成氧化铝保护膜,该选项说法不正确.
故选:D.
(2)①A中细铁丝燃烧生成的黑色固体物质是四氧化三铁,四氧化三铁的化学式是Fe3O4.
故填:Fe3O4.
②B中铁钉最易生锈的部位是b,这是因为b处的铁和水、氧气充分接触.
故填:b.
③C中刚开始无气泡产生,溶液颜色逐渐由无色变为黄色,此时试管内氧化铁和稀硫酸反应生成了硫酸铁和水,发生反应的化学方程式是:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
故填:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
④铁和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式及其质量关系为:
Fe+CuSO4═FeSO4+Cu,
56 64
由以上质量关系可知,当有56份的铁形成溶液的一部分时析出64份质量的铜,因此随着反应的进行,溶液质量减小.
故填:减小.
(3)在AgNO3、Al(NO3)3、Cu(NO3)2的混合溶液中加入一定量的铜粉,固体中一定含有铜和硝酸银反应生成的银,溶液甲中一定含有的阳离子有没有反应的铝离子和铜离子(原溶液中硝酸铜中含有铜离子,反应生成的硝酸铜中含有铜离子).
故填:Ag;铝离子和铜离子.
(4)设锌的质量为x,
反应生成氢气的质量为:10g+40g-49.9g=0.1g,
Zn+H2SO4═ZnSO4+H2↑,
65 2
x 0.1g
$\frac{65}{x}$=$\frac{2}{0.1g}$,
x=3.25g,
原合金中铜的质量分数为:$\frac{10g-3.25g}{10g}$×100%=67.5%,
答:原合金中铜的质量分数为67.5%.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

| A. | 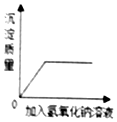 向一定质量的稀盐酸和氯化铜的混合溶液中加入氢氧化钠溶液 | |
| B. | 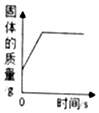 用一氧化碳还原氧化铁 | |
| C. |  等质量镁、锌分别和足量等质量分数的盐酸反应 | |
| D. | 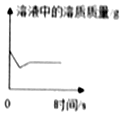 某温度时,向一定量的饱和氢氧化钙溶液中加入少量氧化钙,再恢复到原温度 |
| A. | K2SO4 | B. | CO(NH2)2 | C. | KNO3 | D. | Ca3(PO4)2 |
| A. | 草莓 | B. | 大米 | C. | 鲤鱼 | D. | 豆腐 |
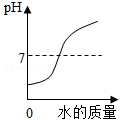 | 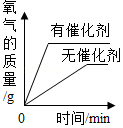 | 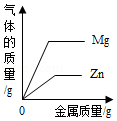 | 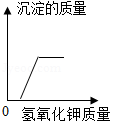 |
| A、向一定量稀盐酸中加水稀释 | B、两份完全相同的过氧化氢溶液分别制取氧气 | C、向两份完全相同 的稀盐酸中分别加入锌粉、镁粉 | D、向盐酸和氯化镁的混合溶液中加氢氧化钾溶液 |
| A. | A | B. | B | C. | C | D. | D |
| 实验步骤 | 实验操作 | 实验现象 |
| 1 | 取样加足量水,充分振荡,静置 | 有白色沉淀产生 |
| 2 | 过滤后,往滤渣中加过量稀盐酸 | 沉淀全部溶解 |
| A. | 该白色粉末中一定含有Ba(NO3)2、Na2SO4、Na2CO3、KNO3 | |
| B. | 该白色粉末中一定含有Ba(NO3)2、Na2CO3,可能含有Na2SO4、KNO3 | |
| C. | 该白色粉末中一定含有Ba(NO3)2、Na2CO3,一定不含Na2SO4、KNO3 | |
| D. | 该白色粉末中一定含有Ba(NO3)2、Na2CO3,一定不含Na2SO4,可能含有KNO3 |
| A. | 白烟 | B. | 火星四射 | C. | 蓝紫色火焰 | D. | 白雾 |
| 气体 | CO2 | SO2 | |
| 制备 | 石灰石与盐酸 | Na2SO3与70%硫酸 | |
| 相似性 | 溶解性 | 能溶于水 | 易溶于水 |
| 与澄清石灰水反应 | 二者都产生白色浑浊 | ||
| 差异性 | 与KMnO4溶液 | 不反应 | 气体被吸收,溶液逐渐褪色 |
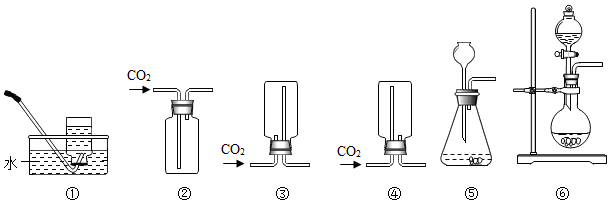
(2)制取CO2的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑,可用于收集CO2装置是②或③.(选填如图序号).
(3)写出Na2SO3与70%硫酸反应的化学方程式Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,制备SO2发生装置用⑥.(选填如图序号).
(4)将收集满SO2的试管倒扣在水中观察到的现象是试管中液面上升.
(5)结合已知信息,请你设计实验证明化石燃料燃烧的气体产物中有CO2(写出操作、试剂、现象、结论)把化石燃料燃烧的气体,先通入足量的KMnO4溶液中,再通入澄清石灰水中,澄清石灰水变浑浊,证明燃烧产物中有二氧化碳.