��Ŀ����
2�����棨Na2CO3���г���һ���������ʣ�ij�������ļ����װ���ϱ��С�Na2CO3������96%��������Ϊ���жϸü�����Na2CO3�ĺ����Ƿ�ﵽҪ��С��ȡ1g�ü�����Ʒ���м��飬���������ɼ�����̵���ƣ��ٶ����ʶ���NaCl������1�������ԭ����ʲô�����û�ѧ����ʽ��ʾ��Na2CO3+BaCl2=BaCO3��+2NaCl��
��2������Ҫ������������̼�ᱵ��������
��3��ͨ������ش𣬵��������������Ƕ���ʱ����Na2CO3������96%������ʵ���ŵģ�
���� ����̼���������Ȼ�����Ӧ������̼�ᱵ������ͨ���ⶨ̼�ᱵ�����������̼���Ƶ��������ɲ��������Na2CO3�ĺ����Ƿ�Ҫ��Ҫ����Na2CO3����������Ҫ����̼�ᱵ����������������̼�ᱵ��������̼���Ƶ����������̼���Ƶĺ�������96%����ô̼���Ƶ�����=1g��96%=0.96g������Na2CO3+CaCl2=CaCO3��+2NaCl���㼴�ɣ�
��� �⣺��1�����Ϸ�����֪������ԭ���ǣ�Na2CO3+BaCl2=BaCO3��+2NaCl��
��2������̼���������Ȼ�����Ӧ������̼�ᱵ������ͨ���ⶨ̼�ᱵ�����������̼���Ƶ��������ɲ��������Na2CO3�ĺ����Ƿ�Ҫ����Ҫ����̼�ᱵ���������������ԣ�ѡ������ҩƷ��ˮ���Ȼ�����Һ��Ӧ������������̼�ᱵ��������
��3�����̼���Ƶĺ�������96%����ô̼���Ƶ�����=1g��96%=0.96g����̼��Ƶ�����Ϊx��
Na2CO3+BaCl2=BaCO3��+2NaCl
106 197
0.96g x
$\frac{106}{0.96g}=\frac{197}{x}$ ��ã�x��1.78g
���������ij��������ݡ�1.78g����Na2CO3������96%��ʱ����ʵ���ŵģ�
���� ������ȿ�����ʵ�鲽�����ƣ��ֿ����˻�ѧ����ʽ����д������ʵ����������ۣ��ۺ��ԱȽ�ǿ��ʵ��̽�����ǽ������п����ȵ�֮һ��������ʵ�鷽�����̵�̽����ʵ����ۺ�ʵ����ɵ�̽���ȣ�����ͨ��ʵ�����Ϻ�ʵ��������õ�����ȷ�Ľ��ۣ����ڽ�����̽����ͬѧ��Ҫ����������ۺ����գ�

 ������������Һ�ж���������ʽ���ڣ�������Ϥ�ĸ��ֽⷴӦ������Һ�����Ӽ��ϵõ�ˮ������������һ�ѧ��Ӧ���磺��������������ķ�Ӧ������Һ�е�H+��OH-��ϳ�ˮ���ӵĹ��̣���ͼ��ʾ���������Ϣ��ͼʾ������Ϊ���и������Ӽ䲻�ܷ�Ӧ���ǣ�������
������������Һ�ж���������ʽ���ڣ�������Ϥ�ĸ��ֽⷴӦ������Һ�����Ӽ��ϵõ�ˮ������������һ�ѧ��Ӧ���磺��������������ķ�Ӧ������Һ�е�H+��OH-��ϳ�ˮ���ӵĹ��̣���ͼ��ʾ���������Ϣ��ͼʾ������Ϊ���и������Ӽ䲻�ܷ�Ӧ���ǣ�������| A�� | H+��Na+��0H-��NO3- | B�� | H+��K+��CO32-��HCO3- | ||
| C�� | Na+��K+��Cl-��OH- | D�� | K+��Ba2+��Cl-��SO42- |
| A�� | �ɴ�����ϼ۸� | |
| B�� | �����ڼ��������Ⱦ�����ƴ������� | |
| C�� | �Ҵ���һ����������Դ | |
| D�� | �����ڴٽ���ʳת�������ũ������ |

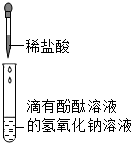 ijͬѧ������ͼ��ʾʵ�飬֤��������Ӧ������Ϊ���Թ�����Һ�ɺ�ɫ��Ϊ��ɫ���÷�Ӧ�Ļ�ѧ����ʽΪNaOH+HCl=NaCl+H2O��ʵ������Թ�����Һ��pH=2������Һ�е����ʳ���̪����NaCl��HCl��
ijͬѧ������ͼ��ʾʵ�飬֤��������Ӧ������Ϊ���Թ�����Һ�ɺ�ɫ��Ϊ��ɫ���÷�Ӧ�Ļ�ѧ����ʽΪNaOH+HCl=NaCl+H2O��ʵ������Թ�����Һ��pH=2������Һ�е����ʳ���̪����NaCl��HCl��
