题目内容
某同学取氯酸钾和二氧化锰混合物15.5g,加热至完全反应得到10.7g固体,问10.7g固体中有哪些物质,各有多少克?
【答案】分析:根据质量守恒定律可知,反应前后固体的质量之差为氧气的质量,然后将氧气的质量代入化学反应方程式来计算氯化钾的质量及二氧化锰的质量.
解答:解:因加热至完全反应,则10.7 g固体中含有氯化钾和二氧化锰,
根据质量守恒定律可知生成氧气的质量为15.5g-10.7g=4.8g,
设生成氯化钾的质量为x
2KClO3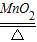 2KCl+3O2↑
2KCl+3O2↑
149 96
x 4.8g
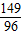 =
=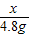
解得x=7.45g
则剩余固体中MnO2的质量为10.7g-7.45g=3.25g
答:剩余固体中含有氯化钾7.45g,含有二氧化锰3.25g.
点评:本题考查学生利用化学反应方程式的计算,明确质量守恒及氧气为气体来计算氧气的质量是解答的关键,然后利用化学反应方程式来计算即可.
解答:解:因加热至完全反应,则10.7 g固体中含有氯化钾和二氧化锰,
根据质量守恒定律可知生成氧气的质量为15.5g-10.7g=4.8g,
设生成氯化钾的质量为x
2KClO3
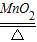 2KCl+3O2↑
2KCl+3O2↑149 96
x 4.8g
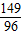 =
=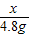
解得x=7.45g
则剩余固体中MnO2的质量为10.7g-7.45g=3.25g
答:剩余固体中含有氯化钾7.45g,含有二氧化锰3.25g.
点评:本题考查学生利用化学反应方程式的计算,明确质量守恒及氧气为气体来计算氧气的质量是解答的关键,然后利用化学反应方程式来计算即可.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目