题目内容
7.向充满CO2的可乐瓶中注入NaOH 溶液,可观察到的现象可乐瓶变瘪了,原因是(用化学方程式示)CO2+2NaOH═Na2CO3+H2O.再注入稀盐酸,可观察到的现象是可乐瓶重新鼓起来,原因是(用化学方程式表示)Na2CO3+2HCl═2NaCl+H2O+CO2↑.分析 根据二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,碳酸钠能与稀盐酸反应生成氯化钠、水和二氧化碳,进行分析解答.
解答 解:向已充满CO2的可乐瓶中注入NaOH溶液,二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,使瓶内压强减小,会观察到可乐瓶变瘪了,化学方程式为:CO2+2NaOH═Na2CO3+H2O;
再注入稀盐酸,碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳气体,使瓶内压强增大,会观察到可乐瓶重新鼓起来,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
故答案为:可乐瓶变瘪了,CO2+2NaOH═Na2CO3+H2O,可乐瓶重新鼓起来,Na2CO3+2HCl═2NaCl+H2O+CO2↑.
点评 本题难度不大,掌握氢氧化钠的化学性质、碳酸钠的化学性质、化学方程式的书写方法是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.维生素C(C6H8O6)主要存在于蔬菜水果,它能促进人体生长发育,增强人体对疾病的抵抗力,近年来科学家还发现维生素C有防癌作用.下列关于维生素C的说法错误的是( )
| A. | 维生素C是有机化合物 | |
| B. | 1个维生素分子有6个碳原子,8个氢原子,6个氧原子构成 | |
| C. | 维生素C中C、H、0三种元素的质量比为3:4:3 | |
| D. | 维生素C中氢元素的质量分数为4.5% |
18.如图所示的实验操作中,正确的是( )
| A. |  倾倒液体 | B. | 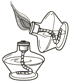 点燃酒精灯 | ||
| C. |  称量氯化钠 | D. |  给固体加热 |
2.加热氯酸钾但不加入二氧化锰,其结果是( )
| A. | 不产生氧气 | B. | 产生氧气的速率减慢 | ||
| C. | 产生氧气的质量减少 | D. | 产生氧气的速率加快 |
16. 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )| A. | 乙一定是化合物 | |
| B. | 丙可能为该反应的催化剂 | |
| C. | 在t1-t2时间段内,四种物质的质量不再改变 | |
| D. | 该反应中,甲、乙的质量变化之比为7:2 |
 水是人及一切生物生存所必需的,我们应该了解有关水的一些知识.
水是人及一切生物生存所必需的,我们应该了解有关水的一些知识.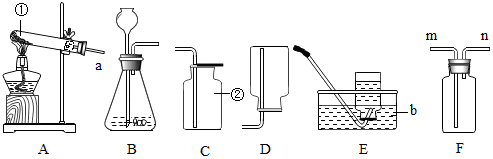
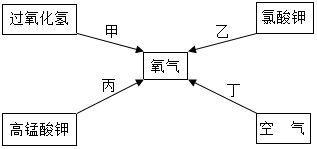
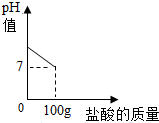 在含氯化钠杂质的纯碱13.6g中逐渐加入质量分数为7.3%稀盐酸,所加稀盐酸的质量关系如图所示:
在含氯化钠杂质的纯碱13.6g中逐渐加入质量分数为7.3%稀盐酸,所加稀盐酸的质量关系如图所示: