题目内容
7.海水的综合利用可以制备金属镁,其流程如图所示: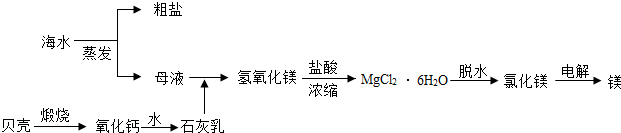
(1)若在空气中加热MgCl2•6H2O,会生成氧化镁,所以要在氯化氢气流中加热MgCl2•6H2O制备氯化镁,分别写出相应反应的化学方程式MgCl2•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$MgO+2HCl↑+5H20↑、MgCl2•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$MgCl2+6H2O↑
(2)上述流程中母液加入石灰乳后,过滤,写出实验室里从滤渣得到纯净氢氧化镁的方法.取样品于烧杯中,加入氯化镁溶液,充分搅拌,过滤,取滤渣,洗涤,晾干.
分析 (1)分析MgCl2•6H2O在空气中加热和在氯化氢气流中加热发生的反应,写出反应的化学方程式;
(2)根据氢氧化镁的表面附着氢氧化钙分析得到纯净氢氧化镁的方法.
解答 解:(1)在空气中加热MgCl2•6H2O,会生成氧化镁,同时生成了氯化氢和水;在氯化氢气流中加热MgCl2•6H2O制备氯化镁,同时生成了水.反应的化学方程式分别为:MgCl2•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$MgO+2HCl↑+5H20↑、MgCl2•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$MgCl2+6H2O↑;
(2)由于向母液加入石灰乳后,过滤得到的氢氧化镁,为了除掉氢氧化镁中的杂质氢氧化钙,应取样品于烧杯中,加入氯化镁溶液,充分搅拌,过滤,取滤渣,洗涤晾干即可得到纯净氢氧化镁.
故答为:(1)MgCl2•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$MgO+2HCl↑+5H20↑;MgCl2•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$MgCl2+6H2O↑;
(2)取样品于烧杯中,加入氯化镁溶液,充分搅拌,过滤,取滤渣,洗涤,晾干.
点评 本题考查海水资源的利用,学生应熟悉粗盐提纯及物质转化中的化学反应并利用信息来综合解答.

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
17.下列物质中,属于纯净物的是( )
| A. | 汽水 | B. | 石油 | C. | 生鉄 | D. | 干冰 |
18.“无土栽培”是一项利用化学试剂配成的营养液来栽培植物的新技术.下列是某营养液所含的主要成分,其中属于复合肥料的是( )
| A. | CO(NH2)2 | B. | Ca(H2PO4)2 | C. | (NH4)2SO4 | D. | KNO3 |
2.环潭中心学校九(8)的章强同学用氢氧化钙和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液中滴加稀盐酸一会儿后,发现忘记了滴加指示剂,因此,他停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行了如下探究.请你和他一起完成探究活动.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】猜想一:溶质只有氯化钙.
猜想二:溶质中有CaCl2和Ca(OH)2.
猜想三:溶液中有氯化钙和氯化氢.
【查阅资料】氯化钙溶液呈中性.
【方案设计】
【方案反思】方案一不能证明猜想一正确的理由是酚酞试液在中性溶液和酸性溶液中都不变色(或盐酸和氯化钙的混合溶液也不能使酚酞变色).
【拓展与应用】实验证明猜想三是正确的.要想使溶液中的溶质只有氯化钙,你认为应该进行的实验步骤是向烧杯中的溶液中加入碳酸钙,直到不再溶解,过滤得氯化钙溶液.
【结论】在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑可能过量的反应物.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】猜想一:溶质只有氯化钙.
猜想二:溶质中有CaCl2和Ca(OH)2.
猜想三:溶液中有氯化钙和氯化氢.
【查阅资料】氯化钙溶液呈中性.
【方案设计】
| 方案 | 方法步骤 | 实验现象 | 实验结论 |
| 方案一 | 取少量烧杯内的溶液于试管中,滴入几滴无色酚酞溶液 | 酚酞不变色 | 猜想一正确 |
| 酚酞变红色 | 猜想二正确 | ||
| 方案二 | 取少量烧杯内的溶液于试管中,逐滴加入碳酸钠(或碳酸钾)溶液至过量 | 开始有气泡产生,后来有白色沉淀生成 | 猜想三正确 |
【拓展与应用】实验证明猜想三是正确的.要想使溶液中的溶质只有氯化钙,你认为应该进行的实验步骤是向烧杯中的溶液中加入碳酸钙,直到不再溶解,过滤得氯化钙溶液.
【结论】在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑可能过量的反应物.
12.下列过程中,一定发生化学变化的是( )
| A. | 玉米酿成酒 | B. | 西瓜榨成汁 | C. | 铁水铸成锅 | D. | 铝块压成箔 |
 某补钙剂说明书的部分信息如图1所示.化学兴趣小组准备测定该补钙剂中有效成分的质量分数,取10片钙片加入稀盐酸至不再产生气泡为止(其他成分既不溶于水,也不与盐酸反应).并绘制了加入稀盐酸的质量与放出气体质量的关系图如图2,则回答:
某补钙剂说明书的部分信息如图1所示.化学兴趣小组准备测定该补钙剂中有效成分的质量分数,取10片钙片加入稀盐酸至不再产生气泡为止(其他成分既不溶于水,也不与盐酸反应).并绘制了加入稀盐酸的质量与放出气体质量的关系图如图2,则回答: