题目内容
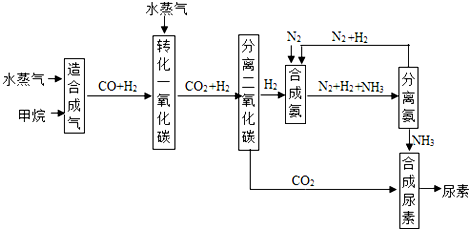
天然气作为三大化石燃料之一,还是极为重要的工业原料.以天然气为原料合成尿素CO(NH2)2的主要步骤如图所示(图中某些转化步骤及生成物未列出):
(1)尿素被称为“氮肥之王”,源于其氮元素的质量分数在各种氮肥中最高,为 ;
(2)合成气生产原理为:甲烷和水蒸气在高温及催化剂的条件下反应,生成CO和H2,该反应的化学方程式为 ;
(3)分离氨的过程为 变化(填“物理”或“化学”;分离出氨后,可循环利用的物质是 .

(1)尿素被称为“氮肥之王”,源于其氮元素的质量分数在各种氮肥中最高,为
(2)合成气生产原理为:甲烷和水蒸气在高温及催化剂的条件下反应,生成CO和H2,该反应的化学方程式为
(3)分离氨的过程为
考点:化石燃料及其综合利用,元素的质量分数计算,化学变化和物理变化的判别,书写化学方程式、文字表达式、电离方程式
专题:化学与能源
分析:(1)计算尿素中氮元素的质量分数;
(2)根据方程式的书写方法进行书写;
(3)根据生产流程图中所涉及的物质的来源和去向回答.
(2)根据方程式的书写方法进行书写;
(3)根据生产流程图中所涉及的物质的来源和去向回答.
解答:解:(1)尿素中氮元素的质量分数:
×100%≈46.7%
(2)反应物是甲烷和水,生成物是一氧化碳和氢气,用观察法配平,反应条件是高温和催化剂,所以方程式是:CH4+H2O
CO+3H2;
(3)分离氨的过程为物理变化,可循环利用的物质是在前面反应中是反应物,在后面的反应中是生成物,分析生产流程图中所涉及的物质的来源和去向发现,N2和H2是循环利用的物质.
故答案为:(1)46.7%;(2)CH4+H2O
CO+3H2(3)物理 N2和H2
| 14×2 |
| 12+16+(14+1×2)×2 |
(2)反应物是甲烷和水,生成物是一氧化碳和氢气,用观察法配平,反应条件是高温和催化剂,所以方程式是:CH4+H2O
| ||
| 高温 |
(3)分离氨的过程为物理变化,可循环利用的物质是在前面反应中是反应物,在后面的反应中是生成物,分析生产流程图中所涉及的物质的来源和去向发现,N2和H2是循环利用的物质.
故答案为:(1)46.7%;(2)CH4+H2O
| ||
| 高温 |
点评:化学来源于生产、生活,又服务于生产、生活,熟悉方程式的书写方法.

练习册系列答案
相关题目
下列变化属于化学变化,并且能用质量守恒定律解释的是( )
| A、5g水受热变成5g水蒸气 |
| B、50mL水加入到50mL酒精中,成为体积小于100mL的溶液 |
| C、木炭燃烧后质量减少 |
| D、10g氢气在8g氧气中燃烧最多生成9g水 |
 2012年4月16日,央视《每周质量报告》报道:九家药企14种胶囊均铬超标,铬在人体内蓄积具有致癌性.铬元素相关信息如图所示:
2012年4月16日,央视《每周质量报告》报道:九家药企14种胶囊均铬超标,铬在人体内蓄积具有致癌性.铬元素相关信息如图所示: 为了测定空气的成分,同学们按如图装置进行了实验.
为了测定空气的成分,同学们按如图装置进行了实验.