题目内容
19. 某盐湖生产的纯碱(Na2CO3)产品中常含有少量的氯化钠(其它杂质忽略不计).为测定该产品中碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g,(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示.
某盐湖生产的纯碱(Na2CO3)产品中常含有少量的氯化钠(其它杂质忽略不计).为测定该产品中碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g,(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示.(1)A点产生气体的质量m=2.2g.
(2)计算试样中碳酸钠的质量分数(结果精确至0.1%).
(3)计算B点时,烧杯内溶液氯化钠溶质的质量分数.
分析 (1)根据产生气体的质量与滴入稀盐酸的质量关系图,A点时碳酸钠与盐酸恰好完全反应,之后再加稀盐酸为过量不再发生反应,因此,根据质量守恒定律,利用最终烧杯内溶液总质量与反应前所加各物质总质量的差值,可求得放出二氧化碳质量;
(2)根据反应的化学方程式,由恰好完全反应放出二氧化碳的质量,可计算样品中所含有碳酸钠的质量,该质量与样品质量比可计算试样中碳酸钠的质量分数;
(3)根据溶质质量分数的计算公式分析解答;
解答 解:(1)根据质量守恒定律,A点产生气体的质量=36.5g+6g-40.3g=2.2g;
故答案为:2.2g;
(2)设样品中碳酸钠的质量为x,生成氯化钠的质量为y,
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
x y 2.2g
$\frac{106}{x}=\frac{44}{2.2g}$
x=5.3g
$\frac{117}{y}=\frac{44}{2.2g}$
y=5.85g
试样中碳酸钠的质量分数=$\frac{5.3g}{6g}$×100%=88.3%
答:试样中碳酸钠的质量分数为88.3%;
(3)B点时烧杯内溶液氯化钠溶质的质量分数:$\frac{5.85g+(6g-5.3g)}{6g+73g-2.2g}×100%$=8.5%;
答:B点时,烧杯内溶液氯化钠溶质的质量分数为8.5%.
点评 分析表示反应规律的曲线时,曲线的折点即图中A点为恰好完全反应,此后所加稀盐酸过量,不再发生反应.

练习册系列答案
相关题目
4.下列说法中正确的是( )
| A. | 某饱和溶液升高温度时,溶液的浓、稀程度不变 | |
| B. | 对于某一溶质来说,饱和溶液比不饱和溶液要浓 | |
| C. | 在某物质的饱和溶液中再加入这种溶质,溶质质量分数增加 | |
| D. | 某物质的饱和溶液加盖密封,当温度变化时,溶液变成不饱和溶液或析出晶体后仍是饱和溶液 |
11.下图所示的实验操作,正确的是( )
| A. | 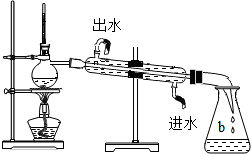 制取蒸馏水 制取蒸馏水 | B. | 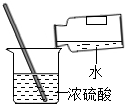 稀释浓硫酸 | ||
| C. | 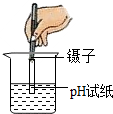 测溶液的pH | D. |  称取氢氧化钠固体 |
8.配制溶质质量分数为80%的甘油溶液500g,所需甘油的质量为( )
| A. | 80g | B. | 40g | C. | 400g | D. | 100g |
9.车祸猛于虎,酒后驾车出事率更高.交警常用一种“酒精检测仪”检查司机是否酒后驾车.其反应原理为C2H5OH+4X+6H2SO4═2Cr2(SO4)3+2CO2↑+9H2O,反应中红色X转化为绿色Cr2(SO4)3,从而知道司机是否饮酒,下列说法错误的是( )
| A. | X的化学式为CrO3 | |
| B. | Cr2(SO4)3中Cr元素的化合价为+3价 | |
| C. | 在反应前后,Cr元素的化合价降低了 | |
| D. | 在C2H5OH中,碳元素与氢元素的质量比为1:3 |
 医生给病人输液时,常用葡萄糖注射液或氯化钠注射液,有时根据病情,也可用葡萄糖复化钠注射液.如图所示的是这种注射液的部分标签.
医生给病人输液时,常用葡萄糖注射液或氯化钠注射液,有时根据病情,也可用葡萄糖复化钠注射液.如图所示的是这种注射液的部分标签.